|
El nivel de concentración se ve
en el hecho de que solo estas primeras 30 presentaciones representan el 12,1%
de las ventas totales y solo las primeras 300 presentaciones de mayor valor
representan el 40,6% del total de ventas reportadas el año 2015. Y el
alto costo, se desprende del hecho de que con solo el 3,9% de unidades
vendidas, las primeras 30 presentaciones toman el 12,1% del mercado en valores
y con solo el 19% de unidades vendidas, las 300 presentaciones más
importantes toman el 40,6% del total del mercado en valores.
2.
De 30 presentaciones
con mayor precio, ninguna está en POS, solo 2 PA no son monopólicos y 1
tiene precio regulado
Al obtener el PUPP-Precio Unitario Promedio de la Presentación como resultado
de dividir el total de ventas en valores reportado por canales
institucional y comercial, entre el total de ventas reportadas en
presentaciones (unidades) también de los canales institucional y comercial,
es posible ordenar lo reportado el 2015 de acuerdo con este criterio (ver
tabla N°2)
|
Tabla N°2: Treinta presentaciones más costosas según Sismed 2015
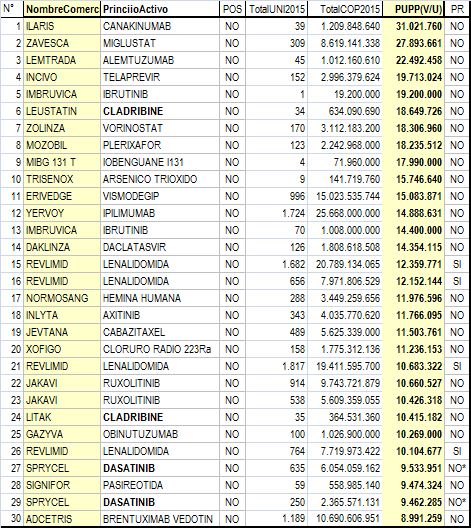 |
| 2.1.
Observaciones: |
1. Casi todas estas presentaciones corresponden a moléculas
monopólicas (varias Biotecnológicas). Solo dos (2)
principios activos tienen un competidor (Cladribine y
Dasatinib) y los competidores no son "genéricos
genuinos" sino "genéricos
con marca" que pueden incurrir en prácticas de
"marca
pionera".
2. Algunos de estos monopolios pueden ser
"reconstruidos" como el caso de Lemtrada
(Alemtuzumab de Sanofi-Genzyme) que siendo monopólico como
Mabcampath para Leucemia Linfocítica Crónica se descontinuó
y reapareció como Lemtrada para Esclerosis Múltiple
Recidivante a precio muy superior. |
3.
De las 30 presentaciones más costosas, ninguna fue incluida
en el POS. Ninguna hizo parte de las "actualizaciones
integrales" del Plan Obligatorio de Salud. Se habrían
entregado con cargo a "recobros" ante el FOSYGA y en
ciertos casos pudieron ser fuente de ingresos adicionales para
las EPS.
4. En ninguno de estos casos existió participación
regulatoria para fijación o negociación de precios. Las
farmacéuticas fijaron precios de entrada a su arbitrio. Solo
en 1 caso -Lenalidomida (Revlimid de Tecnofarma)- se reguló
el precio a-posteriori y en 1 caso -Dasatinib (Sprycel de BMS)
existe PRpUMC. |
| 2.2.
Medidas indispensables: |
2.2.1.
Apertura a la competencia
Urge la entrada en vigencia del Decreto
1782 de apertura a la competencia con medicamentos
biotecnológicos que lleva 5 meses de atraso y urgen
medidas equivalentes para medicamentos monopólicos no
biológicos.
2.2.2. Medidas antimonopólicas
La "reconstrucción" de monopolios (caso Lemtrada) y
construcción perversa de monopolios sobre falsas innovaciones
(caso Daclastavir+Asunaprevir) no está penalizada en
Colombia. Urgen estas y otras medidas antimonopólicas. |
2.2.3.
Medidas regulatorias URGENTES
- Reglamentar Artículo
72 de la Ley 1753 del Plan Nacional de Desarrollo,
- Crear un sistema de fijación o negociación de precios
"a la entrada",
- Faltan verdaderas "actualizaciones integrales" del
POS y "Plan Implícito"
- Falta aplicar la metodología PRI a 30 y más principios
activos no regulados
- Falta generar una metodología que mejore los precios PRI
(Caso Imatinib).
- Transparencia: Creación
un sistema PÚBLICO de información de recobros.
- Implementar la Resolución
de Transparencia (ver Comentarios
Respuestas). |
|
3.
Análisis de
ventas por rango de precios de POS y No-POS permite identificar
tendencias en el gasto de medicamentos
Con el propósito de estimar la estructura del gasto en presentaciones
vendidas POS y No-POS, tomamos en cuenta el PUPP (Precio Unitario Promedio de
cada Presentación, resultado de dividir el total de ventas en COP entre el
total de ventas en unidades) y obtuvimos los resultados que se muestran en la
tablas N°3 y N°4, de presentaciones POS y No-POS respectivamente:
|
Tabla
N°3: Ventas por rango precios Productos
POS s/Sismed
2015
SISMED 2015
no muestra reportes de ventas de productos POS con
precios de los rangos "mayor de 15 millones" y
"De 7 a 15 millones"
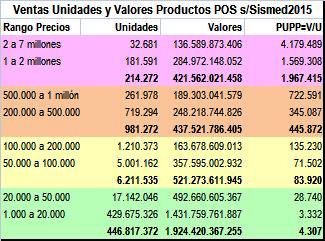 |
3.1.
Observaciones sobre presentaciones POS:
1. Los reportes a SISMED 2015, no muestran Productos POS con
precios superiores a COP 7 millones, es decir, no existen
reportes de Productos POS con precios ">15
millones" y "De 7 y 15 millones" (zona
roja).
Lo anterior implica que el 2015 no existen presentaciones
POS con PUPP superior a 7 millones que se hayan pagado con
cargo a la UPC que administran las EPS. Este
rango no llega a la 3a. parte del No-POS.
2. Las ventas de presentaciones POS del rango de precios
"De 200.000 a 1 millón" (zona naranja) que se
pagaron con cargo a la UPC administrada por las EPS, no
llegaron al 50% de sus equivalentes en presentaciones No-POS.
3. Las ventas de presentaciones POS del rango "De 50.000
a 200.000" (zona amarilla) que se pagaron con cargo a la
UPC administrada por las EPS, no llegaron a la tercera
parte de sus equivalentes en presentaciones No-POS.
4. Las ventas de presentaciones POS del rango "De 1.000 a
50.000" (zona verde) que se pagaron con cargo a la UPC
administrada por las EPS, son de lejos las más importantes
del grupo de presentaciones POS, superan las ventas en
unidades de los No-POS pero son inferiores en valor (menor
precio). |
|
|
Tabla
N°4: Ventas por rango precios Productos
No-POS s/Sismed
2015
 |
3.2.
Observaciones sobre presentaciones No-POS:
1. Los reportes a SISMED 2015, muestran Productos No-POS con
precios de los rangos "Mayor de 15 millones" y
"Entre 7 y 15 millones" que con pocas unidades
generan cifras de negocios muy significativas (zona roja).
Lo anterior implica que el 2015 todas las presentaciones
No-POS con PUPP superior a 7 millones, se pagaron con cargo a
recobros ante el FOSYGA. En este
rango se triplica el valor pagado con cargo la UPC.
2. Las ventas de presentaciones No-POS del rango de precios
"De 200.000 a 1 millón" (zona naranja) que se
pagaron con cargo a recobros ante FOSYGA y gasto de bolsillo
de los pacientes, duplicaron el monto del rango naranja POS.
3. Las ventas de presentaciones No-POS del rango "De
50.000 a 200.000" (zona amarilla) que se pagaron con
cargo a recobros ante FOSYGA y gasto de bolsillo de los
pacientes, triplicaron el monto del rango amarillo de POS.
4.- Las ventas de presentaciones No-POS del rango "De
1.000 a 50.000" (zona verde) que se pagaron con cargo a
recobros ante FOSYGA y gasto de bolsillo de los pacientes, fueron
inferiores a las ventas en unidades de los POS pero bastante
superiores en valores (mayor precio en puntos de venta al
público). |
|
4.
Rangos de precios por tipo mercadotécnico de productos. Tendencias esperadas
con la vigencia de la Ley Estatutaria
Al relacionar los rangos de precios PUPP de los anteriores puntos con la
clasificación mercadotécnica de medicamentos (en "Marcas
Pioneras", "Genéricos con Marca" y "Genéricos
Genuinos") puede verse que las "marcas pioneras" dominan en
todos los rangos de alerta roja, naranja e incluso amarilla. Los
"Genéricos con Marca" aparecen en los rangos menores de alerta roja
y su importancia es creciente en los rangos de alerta naranja y amarilla. Los
"Genéricos Genuinos" solo aparecen en los rangos menores de alerta
naranja, su importancia crece en los rangos de alerta amarilla y se hace
dominante en rangos verdes de menor costo.
| Presentaciones
de Marcas Pioneras |
Presentaciones
Genéricos con Marca |
Presentaciones
Genéricos Genuinos |
| MP dominan
rango de precios >15 millones |
No existen
GM en rango de precios >15 millones |
No existen
GG con precios superiores a 15 millones |
| MP dominan
rango de precios de 7 a 15 millones |
No existen
GM con precios de 7 a 15 millones |
No existen
GG con precios de 7 a 15 millones |
| MP dominan
rango de precios de 2 a 7 millones |
Muy
pocos GM tienen precios de 2 a 7 millones |
No existen
GG con precios de 2 a 7 millones |
| MP dominan
rango de precios de 1 a 2 millones |
Pocos
GM tienen precios de 1 a 2 millones |
No existen
GG con precios de 1 a 2 millones |
| MP dominan
rango de precios 500.000 a 1 millón |
Pocos
GM tienen precios de 500.000 a 1 millón |
No existen
GG con precios de 500.000 a 1 millón |
| MP dominan
rango de precios 200.000 a 500.000 |
Pocos
GM tienen precios de 200.000 a 500.000 |
Muy
pocos GG tienen precios de 200.000 a 500.000 |
| MP dominan
rango de precios 100.000 a 200.000 |
Varios
GM tienen precios de 100.000 a 200.000 |
Muy
pocos GG tienen precios de 100.000 a 200.000 |
| MP dominan
rango de precios 50.000 a 100.000 |
Varios
GM tienen precios de 50.000 a 100.000 |
Pocos
GG tienen precios de 50.000 a 100.000 |
| Pocas MP
tienen precios de 20.000 a 50.000 |
Muchos
GM tienen precios de 20.000 a 50.000 |
Muchos
GG tienen precios de 20.000 a 50.000 |
| Muy pocas
MP tienen precios de 1.000 a 20.000 |
Muchos GM
tienen precios de 1.000 a 20.000 |
Muchísimos
GG tienen precios de 1.000 a 20.000 |
Tendencias esperadas en
estos grupos al entrar en vigencia la Ley Estatutaria de Salud
4.1. Las "marcas pioneras" de la
franja en alerta roja que ingresaron -o ingresarán pronto al mercado- con
precios exorbitantes, mantendrán esa tendencia. En la actualidad el costo de
estos medicamentos está cubierto con recobros al FOSYGA y existen analistas
que suponen que el impacto de la migración del No-POS al pago por UPC será
"indoloro" y hasta podría resultar beneficioso, ya que las EPS
pasarían a ser dolientes y jugar un rol de contención del gasto. Aunque
estos argumentos pueden ser parcialmente ciertos (el ingreso de los primeros
biotecnológicos al POS demostró que eso no sucede) resulta más razonable
para la defensa del sistema, suponer que las redes de prescriptores y
litigantes que las farmacéuticas controlan, mantendrán la dinámica de
crecimiento que mostraron hasta la fecha. Por lo tanto, mientras no se
neutralice la sinergia "debilidad institucional + debilidad regulatoria +
captura de prescriptores y litigantes por las farmacéuticas" los
productos de este grupo mantendrán su tendencia a drenar los recursos del
sistema con ritmo exponencial.
4.2. Los "marcas pioneras" de las
franjas en alerta roja y naranja que ingresaron al POS, también
mantendrán su dinámica de crecimiento. Varios ya demostraron que dicho
ingreso al POS no afectó su ritmo de crecimiento. Los más representativos
neutralizaron los efectos de la regulación de precios e ingreso al POS con
aumentos significativos de sus ventas en unidades.
4.3. Los "marcas pioneras" de las
franjas en alerta naranja y amarilla que actualmente se financian con
recobros, pero en mayor medida con gasto de bolsillo de pacientes, constituyen
la franja que migrará crecientemente del No-POS al nuevo plan de beneficios.
En esta franja -especialmente la amarilla- el gasto No-POS del 2015 fue el
triple del POS y es posible que por lo menos 2 terceras partes de esta franja
presionen su entrega con cargo al sistema (ver caso Antihipertensivos ARA-II o Sartanes
en boletines BisBcm#37
a BisBcm#41
de 2015).
4.4. Los "Genéricos con Marca" de
las franjas en alerta roja, naranja y amarilla, actualmente contribuyen
poco a mejorar el acceso y regular los precios, porque la regulación les
aplica márgenes que corresponden a las marcas pioneras y la desregulación
les induce a prácticas propias de las marcas pioneras. Este rol se mantendrá
en esa dirección si no se encuentran mecanismos concretos para que jueguen el
rol de regulación por competencia que les corresponde (por lo menos a las
farmacéuticas que aún no fueron adquiridas por las multinacionales).
4.5. Los "Genéricos Genuinos" de
las franjas en área verde, reflejan el mayor consumo, tanto en las
presentaciones POS como en las No-POS. Los PUPP de las presentaciones POS de
la última franja corresponden al 50% de su equivalente en las presentaciones
No-POS porque los precios institucionales son inferiores a los comerciales.
Esta sería la única franja que no sufriría mayores modificaciones con la
entrada en vigencia de la Ley Estatutaria.
Por todo lo anterior, puede decirse que -con la
ampliación del plan de beneficios que ordena la Ley Estatutaria- las
"marcas pioneras" y los "genéricos con marca" de las
franjas roja, naranja y amarilla de las presentaciones No-POS ejercerán una
presión colosal sobre la sostenibilidad financiera del sistema de salud. Y el
impacto será superior a las estimaciones que aparecen en las presentaciones
de los Ministerios de Salud y Hacienda, al extremo de que después de todos
los ajustes presupuestales y tributarios que se plantean, el sistema avanzará
inexorablemente hacia el colapso financiero.
5. Ajustes de
más competencia, mayor regulación y mejor prescripción de medicamentos que salvarían el sistema de salud
En el punto 2.2. se resumen las principales
medidas de apertura a la competencia y mayor regulación que el sistema
requiere para evitar que la ampliación del plan de beneficios que dispone la
Ley Estatutaria en Salud precipite el colapso financiero del sistema de salud.
Pero, tal como se planteó en el Boletín#43
de 2015:
5.1. El
Decreto
1782 de apertura a la competencia con medicamentos biotecnológicos está
lejos de ponerse en práctica.
En la página
del Ministerio de salud puede verse el detalle de lo sucedido con el
Decreto 1782 del 18 de septiembre de 2014, la nota oficial de prensa, el Decreto
(AR),
el archivo Abecé medicamentos biotecnológicos
(ARMI)
y la página de Consulta pública proyecto de decreto registro y vigilancia de medicamentos de origen biológicos y biotecnológicos,
con todos los detalles del proceso de su discusión y aprobación. Se publican además del Plan de trabajo para la reglamentación del Decreto
(ARMI);
el Proyecto normativo "Buenas Prácticas De Manufactura de Medicamentos Biológicos"
(ARMI)
del 17 de abril de 2015, con sus Comentarios
y Respuestas
(ARMI);
el Proyecto normativo "Guía de Estabilidad de Medicamentos Biológicos"
(ARMI)
del 11 de mayo de 2015 con sus Comentarios;
el Proyecto normativo "Guía de Inmunogenicidad de Medicamentos Biológicos"
(ARMI)
del 24 de junio de 2015, con sus Comentarios
y la Agenda del Foro Internacional de Proteínas Terapéuticas: Característica Intrínseca, Evaluación
Permanente del 5 y 6 de agosto de 2015 (ARMI).
La situación actual del proceso
de puesta en vigencia del Decreto 1782 se resume en una comunicación
recientemente enviada por el Ministerio de Salud a la Procuraduría General de
la Nación que menciona tres (3) pasos que aún faltan:
1. Deben publicarse las Guías mencionadas, en su versión definitiva,
2. Los reglamentos técnicos deben contar con concepto previo de abogacía de la competencia que emite la Superintendencia de Industria y Comercio y
3. Por ser Colombia signante de la OMC y en cumplimiento de la Ley 170 de 1994, debe realizarse una consulta pública ante la OMC por el término de
3 meses.
En resumen, 5 meses después de cumplido el año previsto por el
mismo Decreto 1782 para la expedición
de las tres Guías necesarias para su implementación, no se ven señales
de que eso vaya a ocurrir pronto.
5.2. Después de la primavera regulatoria del 2013 y una Circular del 2014,
la regulación de precios está detenida.
La página de regulación de
precios de medicamentos del Ministerio de Salud (ver)
muestra que después de la Circular
03 de 2013 que fija la nueva metodología de Precios de Referencia
Internacional PRI, aparecen las Circulares
04 y 05 de 2013, 06
y 07
de 2013 y luego la 01
de 2014, publicada en el Diario Oficial 49111 del día 02 de abril de 2014.
A partir de esa fecha, aparecen
los borradores de Circulares no expedidas:
- La Circular
02 de 2014 (ARMI)
de mayo de 2014 que consolida la regulación vigente sobre precios de recobro, armoniza la metodología contenida en la Circular 03 de 2013 con el método de cálculo de la Circular 04 de 2012 y deroga la regulación previa
- La Circular
02 de 2015 (ARMI)
de enero de 2015 que incorpora medicamentos al régimen de control directo
y autoriza un ajuste de precios por IPC para los regulados en control directo.
Este ajuste fue resuelto con la Resolución 0718 publicada en el Diario Oficial No. 49.452 del 13 de marzo de 2015
"Por la cual se autoriza el ajuste por IPC para los precios de los medicamentos regulados en las Circulares 04, 05 Y 07 de 2013 y 01 de
2014".
- La Circular
03 de 2015 (ARMI)
de febrero de 2015 que compila y unifica los valores regulados para propósitos de reconocimiento y pago por parte del FOSYGA.
Al firmarse la Ley Estatutaria el 16 de febrero de 2015 (ver cronología
en El Pulso), la Comisión Nacional de Precios de Medicamentos y
Dispositivos Médicos (CNPMyDM) resultó eliminada y se generó un vacío
normativo que hasta la fecha no está resuelto. El borrador
de Resolución
"Por la cual se modifica parcialmente la Resolución 0718 de 2015 y se incorporan unos nuevos medicamentos al régimen de control directo de
precios" (en
consulta hasta el 17 de julio de 2015) y el borrador de Decreto
"Por el cual se delegan unas funciones en la Comisión Nacional de Precios de Medicamentos y Dispositivos Médicos"
(en consulta hasta el 10 de agosto de 2015) siguen sin expedirse. La regulación de precios está
detenida.
5.3. No existen políticas públicas de
estímulo a la prescripción médica socialmente responsable, transparencia en
información de recobros y en las relaciones de médicos y litigantes con las
farmacéuticas.
- El INVIMA sigue sin publicar información para prescribir medicamentos y el sistema de información real a prescriptores sigue cooptado por las farmacéuticas.
El Colegio Médico de Cundinamarca y
Bogotá- presentó una acción de tutela para que el INVIMA, -tal como lo
hacen Agencias reguladoras como la FDA, EMA e incluso países vecinos-
publique información oficial para prescribir medicamentos. La tutela fue
negada porque no existía una norma legal que le obligue a hacerlo. Hoy, la
Política Farmacéutica Nacional, la Ley Estatutaria y la Ley del Plan de
Desarrollo, fijan esa obligación, pero el INVIMA hasta la fecha aún no publica
información oficial y completa para la prescripción de medicamentos en
Colombia. La "información para prescribir"
está capturada
por las farmacéuticas y llega a los médicos con adecuaciones de fondo y forma que inducen al
uso de marcas comerciales de precios perversos.
- El sistema de información de precios y ventas de medicamentos a SISMED
funciona pero con inconsistencias que limitan su utilidad. Los errores y ausencias de ATC,
translocación de datos entre canales, reporte simultáneo de las unidades en monodosis y empaques, datos erróneos,
insuficientes y absurdos,
deterioran la calidad de la información que se publica.
- En cuanto a políticas públicas de transparencia, la creación de un sistema
PÚBLICO de información de recobros sigue siendo una necesidad
insatisfecha y sigue sin implementarse la Resolución
de Transparencia (ver Comentarios
Respuestas)
que haga públicas las relaciones financieras de prescriptores y litigantes
con las farmacéuticas que se benefician con sus acciones.
Conclusión: "Sin más competencia, mayor regulación y mejor prescripción, la Ley Estatutaria
de Salud no es
viable" y estamos lejos de implementar los cambios que la viabilidad
financiera del sistema de salud necesita. La Federación Médica Colombiana
y el Colegio Nacional de Químicos Farmacéuticos de Colombia, llaman la
atención sobre la gravedad de esta situación y convocan a todos los actores
de la cadena del medicamento a contribuir con acciones concretas en defensa de
la Ley Estatutaria y el sistema de salud.
Envíe sus aportes y
comentarios a observamed.fmc@gmail.com
o trine en @OBSERVAMED
Sobre
conflictos de interés:
La iniciativa "Elijamos
Sabiamente" de la Federación
Médica Colombiana FMC y el Colegio
Nacional de Químicos Farmacéuticos de Colombia CNQFC, no recibe ninguna retribución monetaria, ni en
especie, de ninguna entidad pública ni privada, que pueda comprometer
la independencia de sus investigaciones e informes.
Participe
escribiéndonos a observamed.fmc@gmail.com
|