|
2. De la desregulación a la regulación por
Valores Máximos de Recobro VMR
En las postrimerías de la
administración de Alvaro Uribe y su ministro Diego Palacio (cuando el
crecimiento exponencial de recobros era un hecho innegable)
dicho
ministro terminó reconociendo
lo erróneo de la política de desregulación total de
precios de medicamentos y su impacto negativo en la crisis
financiera del sector salud.
-
Al finalizar la administración
Urbe-Palacio se intentaron algunas medidas correctivas que
resultaron ser más mediáticas que efectivas. En múltiples
pronunciamientos (Ver BIS-BCM#17, BIS-BCM#18 y BIS-BCM#19)
la Federación Médica Colombiana-FMC insistió en que las
Resoluciones 1424 y
1499, del Ministerio de la Protección Social (que
implementaban el Decreto
1313 de importaciones paralelas) y la Circular
03 de 2010 de la Comisión Nacional de Precios de
Medicamentos (que pasó 925 productos a régimen de
liberta regulada sin precio de referencia),
presentaban inconsistencias por
las cuales no producirían los ahorros prometidos por el
Ministro saliente. La FMC dijo aquella vez que estas
medidas, incluyendo la
Circular 04 de 2010 que fijó Valores Máximos de Recobro-VMR
para 25 productos, la Resolución
1662, que dio reversa y excluyó de la lista de
importaciones paralelas los productos de la multinacional
Roche y la
1663 que añadió otras 8 marcas en dicho listado ya poco
útil, eran parciales e insuficientes y así
fue: El año 2010 los recobros siguieron subiendo y
llegaron a COP 2,4 billones. Ver Infografía
N°1.
-
Al comenzar la administración
Santos (con el ministro Mauricio Santa María y al parecer
por inactividad de la Comisión Nacional de
Precios de Medicamentos-CNPM) se amplió la
regulación de precios basada en Valores Máximos de Recobro-VMR:
Se expidió el Decreto
4474 de 2010 que facultaba al ministerio para fijar dichos
precios máximos y luego las Resoluciones 5229 de
2010; 05, 1020, 3026, 3470 y 4316 de
2011 que la implementaban (la ministra Beatriz Londoño
añadió la
2569 de
2012 que derogó la 4316).
Así, la nueva administración dijo haber controlado los sobreprecios de
163
principios activos, equivalentes al 98% de medicamentos de
mayor impacto en los recobros al FOSYGA. El año 2011 los
recobros alcanzaron a bajar hasta 1,8 billones. Ver
gráfíco
N°1.
-
Pero, abogados afines a las
farmacéuticas afectadas por esta regulación, demandaron el
Decreto 447 ante el Consejo de Estado, que aceptó la
demanda y dejó en el limbo los precios regulados por VMR. Para
superar este vacío regulatorio, la
CNPM expidió la
Circular
04 de 2012 que fue presentada como una gran solución por
los ministerios de
Salud y Comercio,
con titulares como "8.600
nuevos medicamentos a control directo de precios". En
realidad, se trató de un desastre regulatorio que la FMC caracterizó
así:
-
El sistema de regulación basado
en VMR fue parcial e insuficiente. Parcial,
porque afectaba solo a los precios de recobro (y
no a los precios exorbitantes en farmacias). Insuficiente,
porque varios de los precios regulados, seguían siendo
exageradamente elevados en comparación -por ejemplo- con los precios en España
(ver Infografía
N°2). Y la
Circular
04 de 2012 simplemente sumó a los VMR,
el 12% de margen de servicio farmacéutico y los convirtió en
los nuevos Precios Máximos de Venta (PMV). Obviamente las
farmacéuticas abusaron de su posición dominante y terminaron
apropiándose del 12% de aumento y la regulación se limitó a
reducir el margen de los prestadores. Una maniobra que
prácticamente no se registró en ningún medio de
comunicación.
3.
De los VMR-2012 a la regulación
de
Precios por Referenciación Internacional
(PRI)
Detener el proceso de apropiación absurda de
recursos de la salud fue particularmente difícil. Resultó
imposible revertir el crecimiento de los recobros, pero
pudo detenerse temporalmente su dinámica de su crecimiento. Fue imposible
cambiar
la proliferación de prácticas perversas en este campo, pero se
avanzó en cambios estructurales para neutralizarlas.
-
La regulación basada en Precios
de Referencia Internacional (PRI), fue más sofisticada en
términos técnicos. Comenzó con la Circular 03 de 2013, que
definió sus normas y se desarrolló con las Circulares 04,
05, 06 y 07 de ese año, que ajustaron los precios de casi
1.000 presentaciones (en un proceso reconocido por su
transparencia) y concluyó con la Circular 01 de 2014 que
fijó algunos detalles finales como los márgenes para
prestadores.
-
Las limitaciones de la
regulación por PRI se evidenciaron en el proceso de
Declaratoria de Interés Público con fines de Licencia
Obligatoria de Imatinib, cuando el propio Ministerio de
Salud demostró que el “PRI calculado para Glivec sin incluir
precios de competidores” resultaba mucho más elevado que el
“PRI calculado con competidores” y con declaratoria de
interés público, decidió fijar el “PRI con competidores”
para Glivec, un PRI-mejorado que abría la posibilidad de
revisar y mejorar otros precios “PRI-deficientes”.
-
Ante la fijación del
“PRI-mejorado” de GLIVEC, el Ministro Gaviria resistió todo
tipo de presiones, de multinacionales farmacéuticas,
entidades nacionales e internacionales, congresistas,
gobiernos, organizaciones médicas y de pacientes e incluso
funcionarios de la Superintendencia de Industria y Comercio
SIC, que con argumentos varios defendieron el interés
comercial de Novartis. Finalmente, el Ministerio de Comercio (¡!) expidió
el Decreto 670 de 2017 que genera contrapesos de MinComercio
y la SIC para frenar futuras solicitudes de Declaratoria de
Interés Público e impedir que el “PRI-mejorado” pueda
aplicarse a otros productos.
-
La regulación se frenó. Se
redujo a la Resolución 718 de 2015 y Circulares 01 de 2016 y
01 de 2017, que solo fijaron incrementos anuales por IPC
sobre los precios regulados del 2013, mientras permanecían
en consulta pública y sin expedirse, borradores de
Circulares 02 de 2014, 02 y 03 de 2015. En 2017 se publicó
el primer borrador de la Circular 03 de 2017 (con múltiples
inconsistencias) dando inicio a una serie de varios
borradores, 4 consultas públicas y la renuncia del Director
de Medicamentos de MinSalud.
El sistema sigue en crisis, pero con logros en
regulación, apertura de competencia y estímulo a la
transparencia, que siguieron al cambio en la Dirección de Medicamentos,
cuando
volvió la “primavera de la regulación” del 2013:
-
Finalmente se expidió la
Circular 03 de 2017 aunque debió modificarse con la
04 de 2018,
-
Se expidieron los Decretos
433 y
710 de 2018, reglamentarios del Art.72 de la Ley del
PND que establece el control a la entrada para tecnologías
de escasa calidad innovadora;
-
Se expidió la
Circular 06 de 2018 de mejoramiento de reportes de
SISMED;
-
Se expidió la
Circular 07 de 2018 que -además de ajustar precios de
2.528 CUM y 457 principios activos- regula precios al
público (así sea solo de anticonceptivos).
-
Se publicó el proyecto de
Circular 08 de 2018 para el control directo de
medicamentos evaluados por el IETS en cumplimiento de los
Decretos
433 y
710 de 2018 (que finalmente no se expidió por
interferencia del Superintendente de Industria y Comercio
Pablo Enrique Robledo) y
-
Se expidió la
Resolución 2881 de 2018 que crea el Registro de
Transferencias de Valor entre actores del sector salud y la
industria farmacéutica y de tecnologías en salud.
Estas medidas, junto a otras aún más
estructurales como el
Decreto 1782 de 2014 de apertura de la competencia con
Biotecnológicos, la creación y puesta en marcha de la
Administradora de los Recursos del Sistema General de Seguridad
Social en Salud (ADRES) y la implementación de la plataforma
“Mi-Pres” para el manejo administrativo de prescripción No-POS
(hoy No-PBS) y la eliminación de los CTC (aunque requiera
ajustes sobre autonomía médica) conforman una gran “caja de
herramientas” que puede aproximarnos a la utopía de neutralizar
finalmente las prácticas perversas de actores con poder que
amenazan la viabilidad del sistema de salud colombiano.
Dos imágenes de la variación
de precios trimestrales de dos presentaciones de los
biotecnológicos más vendidos y
recobrados en Colombia, sirven para introducir el tema
de la desregulación y posterior regulación de precios de
medicamentos en Colombia. Se trata de Rituximab (Mabthera®)
y Trastuzumab (Herceptin®)
de Roche. Puede verse que, luego de la desregulación de precios de la
administración Uribe, los intentos de regulación (por Valores Máximos de Recobro VMR,
Precios de Referencia Internacional PRI e iInclusiones
al POS hoy PBS)
corresponden a la administración Santos.
Gráfico N° 2:
Impacto diferentes modalidades de regulación en los
precios de dos biotecnológicos más recobrados
Ver
artículo publicado en el periódico EPICRISIS del Colegio
Médico Colombiano (agosto de 2018)
Ver
https://twitter.com/OBSERVAMED/status/1030473173962248192
e
Imagen de la página 15
El Ministro Gaviria en un artículo para El Tiempo
(Competencia
y regulación, puntos vitales en comercio de medicamentos)
escribió “Hemos
ido más allá de la indignación; tenemos método, voluntad y
claridad para enmendar los errores del pasado y acabar, de una
vez por todas, con los abusos del presente”. Los médicos
podríamos profundizar estos logros en el marco de la autonomía
médica y la autorregulación.
4.
Regulación de precios de Medicamentos en las
Administraciones Santos
(2010-2018)
La regulación de precios de medicamentos de la
Administración Santos, fue una de las políticas públicas más
consistentes. Por esta razón, en lugar de intentar una reseña de
las principales medidas que se pusieron en práctica, publicamos
un
ESPEJO de la
página del MSyPS del día 06 de agosto de 2018
VER
Espejo MSyPS 06ago18
RESUMEN EN CONSTRUCCION - RESUMEN EN
CONSTRUCCION - RESUMEN EN CONSTRUCCION - RESUMEN EN
CONSTRUCCION
5.
Hipotonía regulatoria de
Precios de Medicamentos en la
Administración Duque-A.Uribe
La
administración Duque fue recibida con instrucciones específicas
para el ministro Juan Pablo Uribe, contenidas en una carta de
"bienvenida" (El
Espectador 17ago18) firmada por el gremio de las
multinacionales farmacéuticas monopolizantes, las nacionales
opuestas a la regulación de precios y la cámara farmacéutica de
la ANDI que reúne a ambas. Hablando en nombre de toda la
industria, este poderoso grupo de presión, exige neutralizar el
Decreto de apertura de competencia en Biotecnológicos, frenar la
declaratoria de interés público de antivirales de acción directa
Anti-Hepatitis C y anular la ampliación de la regulación a los
precios a la entrada y por valor terapéutico.
En relación
con
el decreto de medicamentos biológicos del 18 de
septiembre de 2014 (https://bit.ly/2B8dXrC)
que regula su registro sanitario "garantizando su seguridad y
eficacia y permitiendo a los pacientes disponer de alternativas
terapéuticas de igual calidad y menor precio" sigue pendiente la
expedición de la "Guía para la evaluación de la comparabilidad
". Se publicó el proyecto normativo y se recibieron comentarios
desde el 30 de Mayo al 21 de junio de 2018. El 11 de julio de
2018 se publicaron los comentarios recibidos y el 15 de agosto
siguiente las respuestas a dichos comentarios. Finalmente el
proyecto debía estar en consulta ante la Organización Mundial
del Comercio - OMC hasta el 2 de noviembre de 2018 para luego
publicarse.
Estamos a punto
de cumplir 5 años de la expedición de la norma y aún la última
guía no se publica y el Decreto de apertura a la competencia de
biotecnológicos aún no puede entrar en vigencia plena.
En cuanto a la Declaratoria de
Interés Público de los Antivirales de Acción Directa para
Hepatitis C, ya pasaron más de 3 años desde que IFARMA presentó
la solicitud y al parecer existen vacíos legales para iniciar
formalmente el proceso. Más allá de los contrapesos del
ministerio de comercio y la SIC que se introdujeron en el
proceso, resulta evidente que ni siquiera pudo adelantarse el
debate técnico con los defensores de los abusos de posición
dominante de las farmacéuticas monopolizantes.
Y el
borrador de la Circular 08 de 2018
(ARMI) que estuvo a punto de expedirse
el 6 de agosto de 2018 culminando la política pública
de definición de precios a la entrada y por valor terapéutico
real. Aquel borrador -promovido por el
ex-ministro Gaviria- buscaba defender la viabilidad
financiera del sistema de salud, frente a la falsa
innovación y los precios exorbitantes con que los
medicamentos sin mayor valor terapéutico ingresan al país.
Ese borrador ya no aparece en la página de
regulación de precios de medicamentos del Ministerio de
Salud, lo cual puede significar que el nuevo MinSalud ya
cedió a las
presiones de las farmacéuticas y está abandonando "La
gran regulación de precios de medicamentos que se cayó a
último minuto" como tituló El Espectador.
Al margen de todo lo anterior,
la hipotonía regulatoria de precios
de medicamentos de la actual administración, se traduce en 4 medidas
de transición:
RESUMEN EN CONSTRUCCION - RESUMEN EN
CONSTRUCCION - RESUMEN EN CONSTRUCCION - RESUMEN EN
CONSTRUCCION
5.1.
Circular 07 de 2018
(ARMI)
El 3 de diciembre de 2018 el gobierno anunció su entrada en
vigencia el 1 de enero de 2019 dando por
concluido el pulso con farmacéuticas que buscaban su derogatoria
parcial o total (ver contexto en ¿Por
qué el Minsalud tuvo que ratificar la regulación de precios de
los anticonceptivos? en El Espectador). Por lo tanto, la
primera regulación que afectó los precios de un grupo de
productos (anticonceptivos) a nivel de intermediarios y
precio público en farmacias, quedó en firme, pese a toda la
oposición de los afectados y sus vínculos gremiales,
diplomáticos e institucionales. Esta Circular entró en vigencia
el 1° de enero de 2019 y aunque no es real que las 902
presentaciones con precio regulado estén efectivamente
disponibles y que los ahorros para el sistema de salud lleguen a
360.000 millones, queda el antecedente de la posibilidad real de
llevar la regulación a los precios al público como lo permite la
Ley Estatutaria de Salud.
5.2.
Circular 08 de 2018 (ARMI)
Expedida el 28 de diciembre de 2018, modifica la
Circular 07 de 2018
(ARMI)
y regula 118 presentaciones, de las cuales, solo 11 presentan
informes de precios y ventas a SISMED (es decir, están realmente
disponibles). estos 11 precios regulados
resultaron superiores a Precio Promedio de la Presentación en Sismed (PPPS) y a precios al público (PPE) NOTA: Como ya
se dijo, esta Circular
no debe confundirse con el borrador del mismo número
(ver), que estuvo a punto de expedirse
el 6 de agosto de 2018 culminando la política pública
de definición de precios a la entrada y por valor terapéutico
real.
|
Precios Regulados de Circular 08 de
2018 versus Precios Sismed y Público
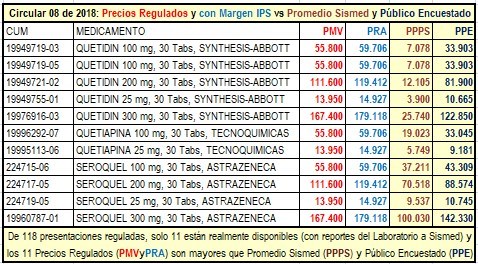 |
Según Observamed-FMC, la nueva Circular 08 de 2018 se convirtió
en un simple listado de rectificaciones de
116 CUM de Quetiapina en
la Circular 07 de 2018, de los cuales solo 11
están disponibles (solo 11 tienen precios
y ventas reportadas por Laboratorios a SISMED) y en los
11 casos, los Precios Regulados (PMV) y con ajuste del
7% para prestadores (PRA) son mayores que el Precio Promedio
Promedio de la Presentación en Sismed (PPPS) y el Precio
Público Encuestado (PPE). Es decir, se trata de una
Regulación que no regula.
Adicionalmente, la nueva Circular 08 plantea
algunas interrogantes legales sobre los datos
consignados en la base de datos del INVIMA:
- ¿Es legal que el logo
sea de ABBOTT cuando en el Registro sanitario y la Circular
08 el producto pertenece a SYNTHESIS?
- ¿Puede la Circular 08
regular un precio de DRUGTECH de SYNTHESIS cuando en
farmacias y droguerías se conoce como QUETIDIN de ABBOTT?
Ver https://bit.ly/2SU3jJw
- Aún cuando Abbott haya comprado a Synthesis
hace varios años ¿afectan o no a la regulación
estas inconsistencias en marcas registradas y
titulares de las mismas? |
|
5.3.
Circular 09 de 2019
Expedida el 8 de mayo de 2019, solo modifica el artículo 1°
de la Circular 07 de 2018 e incorpora al régimen de control
directo los anticonceptivos QLAIRA de Bayer y EVELY de Lafrancol
y modifica el artículo 5° de la misma Circular adicionando el
numeral 327 con Dienogest y Valerato de estradiol (ver).
Estuvo en consulta varios meses y entrará en vigencia 2 meses
después de su publicación en el Diario Oficial.
5.4.
Resolución 1019 de 2019
La Resolución 1019 expedida el 2 de mayo de 2019
(ver)
fija Valores Máximos de Recobro VMR para 50 principios activos.
Difiere del proyecto publicado por esta misma administración (ver)
que incluía 105 principios activos de alto impacto que no fueron
afectados por la regulación de precios por referencia
internacional PRI, el cual a su vez, difiere también del
proyecto original de 2018 (ver)
que no incluía ningún listado de principios activos, pero era
más explícito en la metodología.
Al tratarse de una "Resolución" del Ministerio de
Salud para establecer los valores que podrán reconocerse en los
recobros pagados por ADRES y no una "Circular" de la Comisión
Nacional de Precios de Medicamentos que establece otra
regulación, se espera que no pueda ser demandada ante el Consejo
de Estado, como sucedió con los VMR de 2012. Falta aún saber la
actitud que adoptarán los diferentes actores afectados.
Al presentar esta resolución, la nota de prensa
de MinSalud antetitula "Por primera vez en la historia, un
Gobierno les pone techo a los valores que las entidades le
cobran a la Nación por suministrar tecnologías y procedimientos
a los colombianos que no se financian a través de la UPC" (ver)
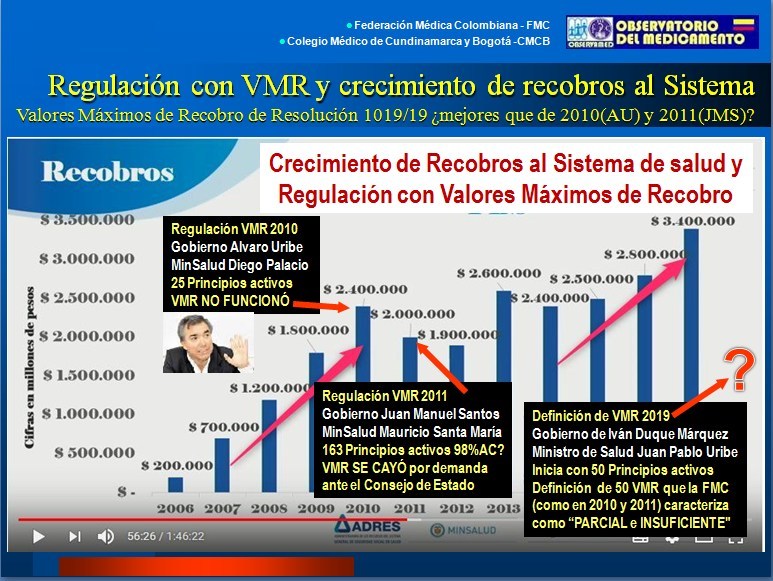
afirmación que no corresponde a la verdad, porque los primeros
VMR se expidieron el 2010 en las postrimerías de la
administración Uribe-Diego Palacio y también el 2011 al iniciar
la administración Santos-Mauricio Santa María (ver gráfico
N°3).
6.
Los VMR de 2019: De la hipotonía regulatoria a la entrega de
recursos a las EPS
A continuación se somete a consulta
pública el borrador
de la Circular 08 de 2018, "Por la
cual se establece la metodología para el control directo
de los precios de los medicamentos para los cuales el
IETS haya realizado una evaluación de valor terapéutico
y económica, según lo establecido en el Decreto 488 de
2017, modificado por el Decreto 710 de 2018 ". Se
recibirán comentarios entre el jueves 21 de junio de
2018 al jueves 12 de julio de 2018 al correo
circ_cnpmdm@minsalud.gov.co. Por favor, en el asunto del
correo indicar que los comentarios se refieren al
proyecto de Circular 08 de 2018.
https://bit.ly/2P7Ubzs
RESUMEN EN CONSTRUCCION - RESUMEN EN
CONSTRUCCION - RESUMEN EN CONSTRUCCION - RESUMEN EN
CONSTRUCCION
Gráfico N°3:
Crecimiento exponencial de recobros y Valores Máximos de
Recobro de 2010-2011 y 2019
Además, la nota dice que "cerca de 1.600
medicamentos hacen parte de este primer conjunto" lo cual
tampoco corresponde a la verdad, puesto que cruzando la lista de
principios activos de la Resolución 1019 con los reportes de
precios y ventas a SISMED puede verse que solo 203 CUM
(presentaciones) de este conjunto se encuentran efectivamente
disponibles en el mercado.
Al relacionar los VMR de la Resolución 1019 con
los VMR de 2010 y de 2011
(ver detalles en
punto 2)
puede verse que en los tres casos pueden
caracterizarse como son “parciales e insuficientes”, "parciales"
porque no afectan los precios exorbitantes para el bolsillo de
los pacientes, e "insuficientes" porque no logran grandes
reducciones de precio que generen ahorros significativos para el
sistema de salud.
Un par de ejemplos con VICTOZA (ver gráfico N°4)
y ULTIBRO (ver gráfico N°5) permiten confirmar esta apreciación:
-
En el caso de LIRAGLUTIDA -que NovoNordisk
promociona para tratamiento de diabetes (VICTOZA) y para
adelgazamiento (Saxenda)- puede verse que el Precio
Promedio de la Presentación en Sismed (PPPS) -de una pluma de
Victoza por 3 mL- es $170.981, el VMR fijado por la
Resolución $174.980 y el Precio Público Encuestado en 5
cadenas de droguerías (PPE) $ 192.890. Por lo tanto, al
multiplicar las 37.217 prescripciones de LIRAGLUTIDA en
MiPres de 2018 (asumiendo que cada prescripción es para 1 pluma)
ADRES ahorraría solo $ 666 millones, mientras que por
354.072 plumas no prescritas en MiPres (convirtiendo todas
las presentaciones de Victoza y Saxenda a 1 pluma y sin poder
diferenciar recobros no registrados via MiPres) los pacientes
pagarían 6.341 millones como mayor valor, por no
estar beneficiados con el precio VMR.
-
En el caso de GLICOPIRRONIO + INDACATEROL -que
Novartis promociona como ULTIBRO con indicación de
broncodilatador en casos de EPOC- puede verse que el Precio
Promedio de la Presentación en Sismed (PPPS) es $105.361,
el VMR fijado por la Resolución es $165.891 y el Precio
Público Encuestado en 5 cadenas de droguerías (PPE) $118.422.
Por lo tanto, al multiplicar las 37.217 prescripciones de
GLICOPIRRONIO+INDACATEROL en MiPres de 2018 por el VMR de la
Resolución 1019, ADRES pagaría $1.460 millones más que
pagando el precio encuestado en 5 cadenas de droguerías.
Entonces ¿dónde está el beneficio de este VMR?
|
Gráfico N°4:
Análisis VMR de Res.1019 con VICTOZA
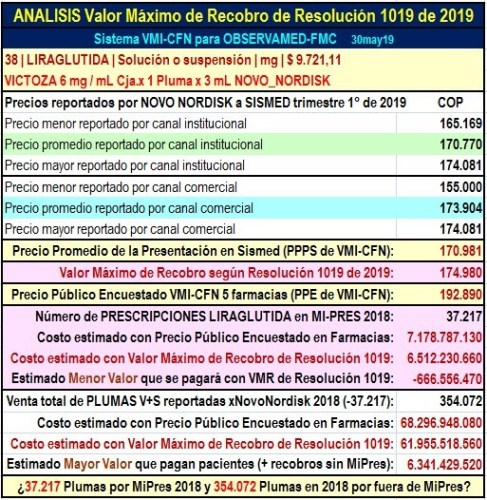 |
Gráfico N°5:
Análisis VMR de Res.1019 con ULTIBRO
 |
Por estos hechos, puede decirse que el error
estructural de estos VMR está en que se basaron en precios de
recobros que históricamente fueron perversos.
Adicionalmente,
al analizar los nuevos VMR, en relación con el dato de
prescripciones del cubo de MiPres, se abren nuevos
interrogantes: Por ejemplo, AGALSIDASA ALFA de Shire-Baxalta
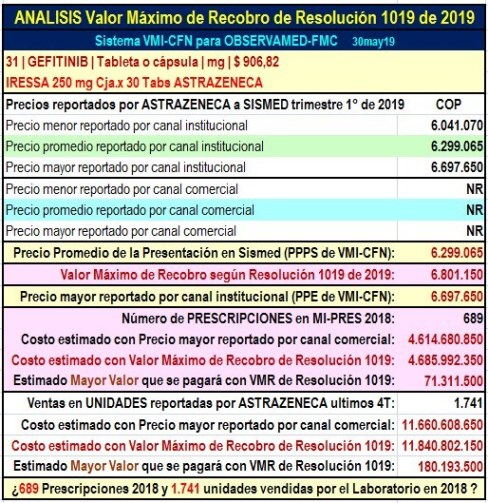
(gráfico N°6) y GEFITINIB de AstraZeneca (gráfico N°7) suman
823 prescripciones en MiPres 2018 y las unidades que no
fueron prescritas en MiPres llegarían a 5.829, por un
valor de $26.244 millones. AGALSIDASA ALFA sola (REPLAGAL
de Shire-Baxalta) tiene 134 prescripciones en MiPres de
2018, pero el Laboratorio reportó la venta de 4.911
unidades en los últimos 4 trimestres. Entonces ¿qué está
pasando? ¿Cuál es el valor de los recobros NO prescritos en
MiPres y cual el mecanismo que se emplea? La necesidad de estas
respuestas vuelve casi irrelevante que lo prescrito en MiPres
con los dos productos costaría 31.465 millones y el
ahorro con VMR sería solo 249 millones.
|
Gráfico N°6:
Análisis VMR de Res.1019 con REPLAGAL
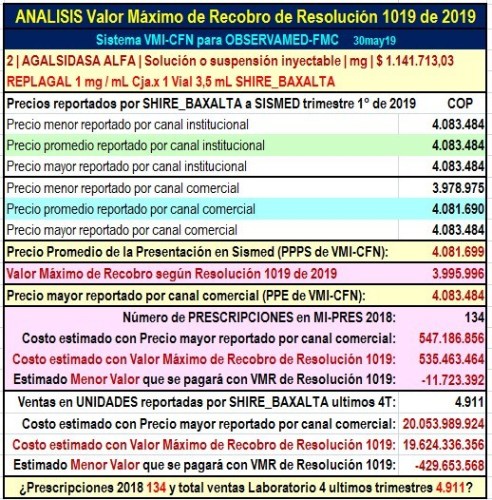 |
Gráfico N°7:
Análisis VMR de Res.1019 con IRESSA
 |
Por lo tanto, la nota de prensa de MinSalud no
debería magnificar tanto unos VMR que ni son nuevos ni tan
eficientes para generar ahorros al sistema de salud.
Sin duda, hacen falta medidas regulatorias mucho
más eficientes como la regulación por precios de referencia
internacional PRI, la declaratoria de interés público DIP para
medicamentos de alto impacto (así sea solo para fijarles un PRI
"con competidores" como sucedió con Glivec), la regulación hasta
el final de la cadena para beneficiar a pacientes (como sucedió
con los anticonceptivos) y la fijación de precios a la entrada y
por valor terapéutico como se planteaba en el borrador de la
Circular 08 de 2018 (ver)
que estuvo a punto de ser expedida por la anterior
administración y hoy no aparece en las páginas de
MinSalud.
7. Observamed-FMC:
Ajustes indispensables en la regulación de precios
Los gráficos de
Rituximab (Mabthera®)
y Trastuzumab (Herceptin®)
de Roche que se muestran antes del punto 4 de esta página
sugieren
que la regulación de precios, seguramente fue la
política pública más exitosa de la admnistración Santos que
-luego de varios intentos- logró resultados notables con
productos institucionales (e incluso algunos medicamentos que
afectan el gasto de bolsillo de los pacientes). Pero la siguiente
diapositiva del último informe ADRES muestra una realidad
preocupante:
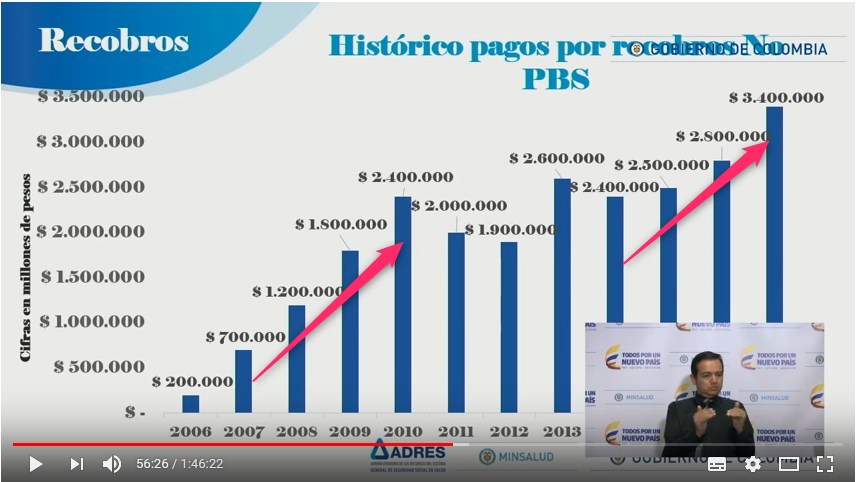
Gráfico N°3:
Crecimiento exponencial de recobros y Valores Máximos de
Recobro de 2010-2011 y 2019
|
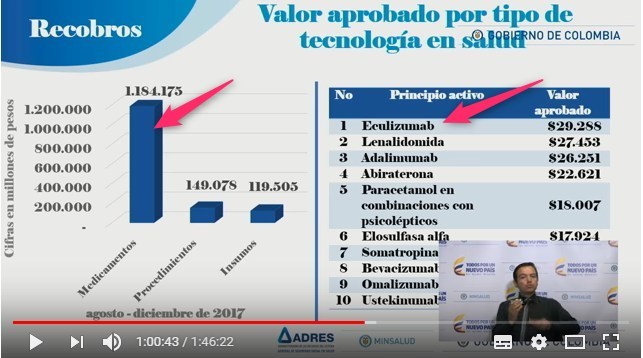
Gráfico N°8:
Moléculas más recobradas en período agosto-diciembre
2017
 |
El crecimiento exponencial de recobros,
que había sido detenido en los años 2012 a 2014, volvió
a dinamizarse y pasó de 2,4 billones en 2014 a 3,4
billones en 2017 con la posibilidad de alcanzar los 4,4
billones en 2018. ¿Cómo explicar que pese al control de
precios de medicamentos No-POS (PBS no financiado con
UPC) de mayor
impacto, los recobros vuelvan a la misma dinámica
creciente?
La
primera parte
de la explicación puede verse en
otra diapositiva de la misma presentación del Informe
ADRES donde se observa que
el peso del componente
"Medicamentos" en los recobros, sigue siendo el más importante y
que en el listado de los principios activos más
recobrados, aparecen nuevos biotecnológicos no regulados
que reemplazaron a los exitosamente regulados.
Además
aparecen varios medicamentos
regulados que, pese a haber sido incluidos en el POS
(hoy PBS) siguen recobrándose en indicaciones que no
fueron incluidas.
Por
lo tanto la primera sugerencia tiene que ver con la
profundización de la regulación, es decir regular
mejor y más rápidamente los medicamentos no regulados de mayor
impacto y eliminar el fallido sistema de inclusión
parcial al POS-PBS "por indicaciones". |
Luego,
al analizar los precios reportados a SISMED y aplicar el concepto de
"Precio Promedio de Presentación en Sismed PPPS"
puede verse que el PPPS o
precio promedio real reportado por los laboratorios (que resulta de dividir el total
de ventas en valores reportado por el laboratorio, por canal
comercial e institucional, entre el total de las ventas en
unidades en ambos canales) muestra relaciones diferentes con el
precio regulado, cuando se trata de "marcas pioneras",
"competidores con marca" o "genéricos genuinos" según la
nomenclatura mercadotécnica propuesta por OBSERVAMED-FMC y
el Colegio Nacional de Químicos Farmacéuticos de Colombia CNQFC.
|
Gráfico N°9:
Precios Regulados vs Reportrados Pregabalina
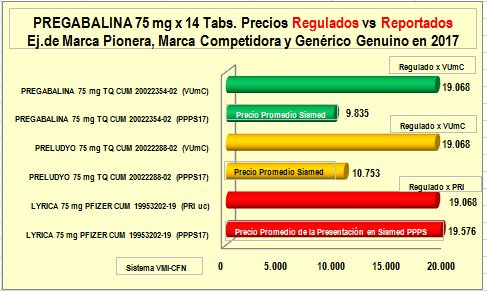 |
Por
ejemplo, si tomamos
Pregabalina -el
principio activo más prescrito (y recobrado) con el aplicativo
MiPres- y comparamos el "precio Regulado por PRI" con el
PPPS de
la “marca pionera” y el precio regulado por Valor de
unidad mínima de concentración (VUmC) con el PPPS de una
“marca competidora” y un “genérico genuino” puede verse que:
a)
La “marca pionera” muestra un PPPS
igual al precio regulado por PRI
b)
La
“marca competidora” muestra
un PPPS muy inferior al precio regulado por VUmC
(que es igual al precio regulado por PRI) y
c)
El “genérico genuino” muestra
un PPPS también muy inferior al precio regulado por VUmC
o PRI.
Esto permite plantear la hipótesis de
"efecto murciélago selectivo" en los recobros con marcas
competidoras e incluso genéricos que el sistema paga al
precio regulado de la marca pionera. Así, ciertos actores
(EPS y prestadores recobrantes) podrían estar apropiándose
del ahorro que debería beneficiar al sistema y
reflejarse en una disminución del volúmenes recobrados.
Así se estaría generando una “propensión
al precio regulado mayor” que aunque no beneficia
directamente a las farmacéuticas, podría ser usado como
argumento de venta de las marcas competidoras y
los genéricos genuinos. |
Por
lo tanto, la siguiente sugerencia tiene que ver con el
"PRI-mejorado", es decir regular precios incluyendo en las
comparaciones la oferta disponible y no únicamente la marca
pionera tal como se hizo con el precio de Imatinib, luego de
la declaratoria de interés público. Frente a las complejidades
de este mecanismo la actitud no puede ser el abandono de la
regulación, sino encontrar la forma de individualizar mejor
la regulación, para que se traduzca en ahorros para el
sistema y no en estímulo para nuevas prácticas perversas.
A propósito de una mejor individualización,
la “regulación PRI-VUmC, por concentración (mg)”
debe ajustarse para las presentaciones hospitalarias multi-unitarias
que con el sistema actual resultan con precios absurdamente
elevados.
Otras sugerencias que no se detallan por cuestión de espacio,
tienen que ver con los precios de los medicamentos para
enfermedades huérfanas, la regulación por grupo terapéutico y
estímulos a la producción nacional.
Gráfico N°10:
No reporte del Laboratorio y Reportes de Mayoristas por
COP 338.200 millones entre 2015 y 2017

Gráfico N°11:
Sistema de salud contuvo costos de IMATINIB por los
perdió con NILOTINIB y DASATINIB
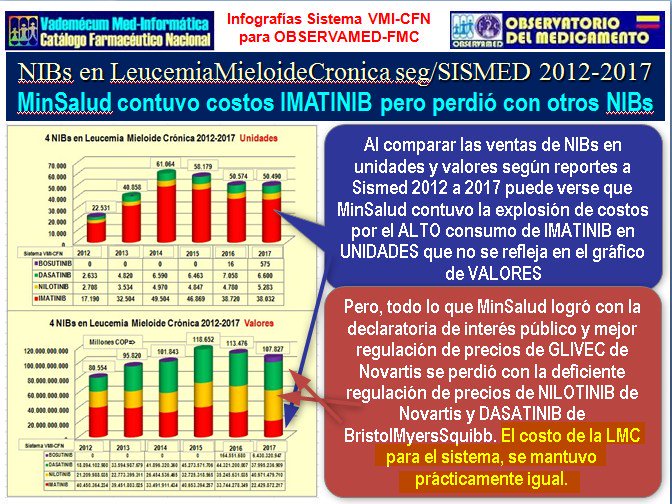
Gráfico N°12:
Medicamentos importados: Con el 27% en unidades se
llevan el 65% de los recursos

EN CONSTRUCCION -
EN CONSTRUCCION - EN CONSTRUCCION - EN CONSTRUCCION -
RESERVA DE ENLAcES DE INTERES - RESERVA DE
ENLACES DE INTERES - RESERVA DE ENLACES
1.1. Tendencias globales: Consenso de
Washington y su aplicación en Colombia
El Artículo 48 de la Constitución
Política de 1991 abrió la puerta al manejo de la
Seguridad Social Pública por el sector privado. El
Congreso de esa época –por iniciativa del gobierno de
César Gaviria y su Ministro de Salud Juan Luis Londoño
De La Cuesta- aprobó la Ley 100 de 1993 que creó las
Empresas Promotoras de Salud (EPS) y Fondos Privados de
Pensiones y Cesantías.
Durante los años
2003-2010, se aplicaron en Colombia políticas públicas
de liberalización a ultranza con desregulación total y
privatización de la Seguridad Social Pública.
Entre otros
efectos, esta política generó el crecimiento exponencial
de recobros al FOSYGA y una apropiación obscena de
recursos de la salud por parte de empresas farmacéuticas
con productos monopólicos de alto costo, junto a algunas EPSs
que montaron una verdadera “industria de recobros”.
En este
período –que la FMC llama octenio de la desregulación-
los recobros al Fosyga por tecnologías “No-POS” pasaron
de 4.244 millones a 2.236.120 millones (2,2 billones),
con un alto componente de “medicamentos” que se recobraron
“a cualquier precio”.
1.2. Apuntes sobre la liquidación del ISS
El Instituto de Seguros Sociales (ISS),
Instituto Colombiano de Seguros Sociales, o Seguro
Social, fue una entidad pública creada el 26
de diciembre de 1946 encargada
de la seguridad
social, principalmente de los empleados del sector
privado con empleo formal.
Funcionó bajo cuatro negocios de la Salud: Entidad
Promotora de Salud (EPS) junto a una red de Clínicas
y Centros de Atención Ambulatoria (CAA), es decir, Instituciones
Prestadoras de servicios de Salud (IPS); asimismo
con Pensiones y
la Administradora
de Riesgos Profesionales (ARP).
El proceso de desaparición y liquidación
de la entidad se inició en 1990,
previo a la nueva constitucionalidad colombiana (ver Constitución
de Colombia de 1991). Este proceso fue abanderado
por una serie de políticos, entre ellos, el presidente
de turno
Cesar
Gaviria Trujillo (1990-1994) y el que sería próximo
presidente, Alvaro
Uribe Velez(2002-2010) quien haría realidad todas
estas políticas de privatización a
través de la ley 50 de 1990 y la ley
100 de 1993. Así, se aplicó el "recetario
económico" del Fondo
Monetario Internacional (FMI) en relación con la privatización de la Seguridad
Social Pública según lo planteado por el Consenso
de Washington
En 2007 fueron
privatizadas todas las IPS de la entidad en todo el
país. En 2008 se
privatizó la EPS y la ARP, quedando sólo con el negocio
de las pensiones.
En 2012 el
Instituto de Seguro Social dejó de existir, siendo
sustituido por Colpensiones en
la administración de las pensiones de los afiliados en
el régimen de prima media.
Cinco de las 10 recomendaciones del
"Consenso de Washington" afectaron el precio de los
medicamentos:
-
Liberalización del comercio: liberación de las
importaciones, con un particular énfasis en la
eliminación de las restricciones cuantitativas
(licencias, etc.); cualquier protección comercial
deberá tener aranceles bajos
y relativamente uniformes;
-
Liberalización de las
barreras a la inversión
extranjera directa;
-
Privatización de las empresas
estatales;
-
Desregulación: abolición de regulaciones que
impidan acceso al mercado o restrinjan la
competencia, excepto las que estén justificadas por
razones de seguridad, protección del medio ambiente
y al consumidor y una supervisión prudencial de entidades
financieras;3
-
Seguridad jurídica para
los derechos
de propiedad.3
Desde 1990, Uribe Vélez fue el promotor
(antes de la expedición de la Constitución Política
de 1991) de los procesos
de privatización de la Seguridad Social Pública,
entendida ésta como los riesgos
en salud, profesionales, cesantías y pensiones.
El último capítulo del
Proyecto de Ley, hoy Ley 50 de 1990, contenía un
articulado final que liquidaba
la seguridad social pública y daba paso al manejo
financiero de ésta por el sector
privado pero, en buena hora, el Congreso de la
República de la época no lo
aprobó y tuvo que esperar hasta la Constituyente
del 91.
La Constitución Política de 1991, en su Artículo
48, permite el manejo de la
Seguridad Social Pública por el sector privado y,
en desarrollo de ésta, se expide
por parte del Congreso y a iniciativa del
Gobierno de la época, el Liberal César
Gaviria, y su Ministro de Salud, Juan Luis
Londoño De La Cuesta, la hoy vigente
Ley 100 de 1993 que crea los Fondos Privados de
Pensiones y Cesantías y las
denominadas Empresas Promotoras de Salud (EPS).
El ministro Juan Luis Londoño de la Cuesta, al
momento de ser aprobada la Ley
100, fue claro en sus declaraciones y exclamó “bienvenidos
al negocio de la
Salud”, parafraseando al entonces Presidente
Gaviria con su frase
“bienvenidos al futuro”.
La Ley 100 de 1993, tuvo tres
propósitos claros: privatizar
la Seguridad Social Pública,
entregando los recursos al sector financiero
especulativo nacional e
internacional, liquidar la Red Pública
Hospitalaria que se venía construyendo en
el esquema del Sistema Nacional de Salud y
entregar el sistema pensional a los Fondos Privados de
Pensiones y Cesantías.
Sangre y componentes anatómicos
CRONOLOGIA
|