|
|
https://www.med-informatica.net/BIS/Especiales/HepatitisC.co.htm
Hepatitis C/Colombia
MinSalud.co/Hepatitis |
Plan Nacional Control HV
Papel de EAPB |
INS Vigilancia HByC
Informes
Evento HB-C-D:
2015
2016
2017
2018
2019
PE-XII-20
PE-XIII-20
HVCo 2015-18
Guía de Práctica Clínica 2018
Presentación |
Vía Clínica Tratamiento Hepatitis C 2018
Archivos Día Mundial Hepatitis:
2017
2018
2019 | Informes Cuenta Alto Costo:
2018
2019
CAC 2019 |
MinSalud Procesos de Declaratoria de Interés Público Hepatitis C
- Imatinib
Seguimiento a DIP
para LO de AAD VHC
|
Resolución
MinSalud 1692 de 2017
Resolución 1692 de 2017: Varias ganancias ¿un par
de pérdidas?
1.
Tres "innovaciones" terapéuticas ya descontinuadas y dos en camino
2.
Hepatitis C primera política pública de compras centralizadas
3.
Futuro de las compras centralizadas e innovación tecnológica para
Hepatitis C
4.
Compra centralizada de medicamentos para Hepatitis C (espejo MS
06ago18)
*Resolución 1692 de 2017: Varias
ganancias ¿un par de pérdidas?
La
Resolución 1692
del 23 de mayo de 2017, constituye un sólido
documento de política pública, por las medidas que
adopta para la prescripción, compra centralizada,
distribución y suministro de medicamentos para la
Hepatitis C crónica. Su anexo técnico establece un
sistema de información para la
identificación de pacientes, diagnósticos y
tratamientos, que -con participación de la
Cuenta de Alto Costo- está generando
mayor control, aunque éste no sea suficientemente
transparente.
Ventas Antivirales AntiHepatitisC - Unidades y Valores - s/Sismed
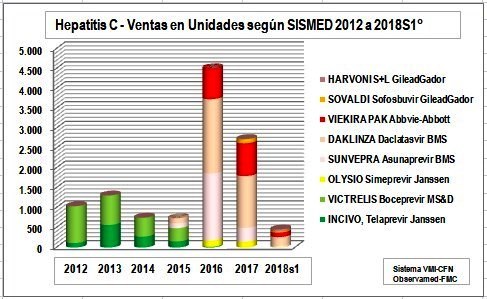
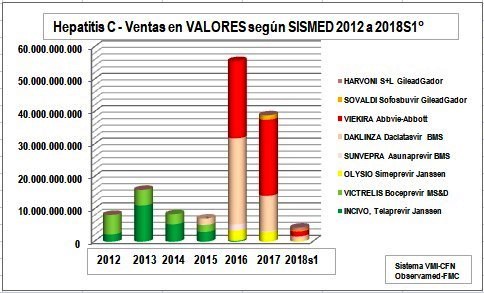
La drástica disminución de las ventas de 2018
en unidades y valores, se debe a que corresponde a solo el
semestre 1°, junto con una evidente desviación de la prescripción hacia
los productos incluidos en la compra centralizada y una pérdida
de la transparencia en la información (que ahora debe obtenerse
vía derechos de petición). Tanto los informes de MinSalud como los de la Cuenta de Alto Costo CAC no son ni
completos ni periódicos. Además, la compra centralizada es
una solución "coyuntural", que está siento usada como argumento para bloquear
soluciones estructurales como la
Declaratoria de Interés Público con fines de Licencia
Obligatoria.
|
|
|
-
Tres
"innovaciones"
terapéuticas ya descontinuadas y
dos
en
camino
(gran parte de este texto fue publicado en
Epicrisis del CMC)
Cinco Antivirales anti-Hepatitis C se llevaron casi
130.000 millones, en ventas reportadas por 5
multinacionales farmacéuticas, antes de que el
Ministerio de Salud logre diseñar y llevar a la
práctica la primera política pública de compras
centralizadas y manejo integral de una patología:
Hepatitis C (ver Tabla N°1 y N°2)
Ventas Antivirales AntiHepatitisC - Unidades y Valores - según Sismed
(Tablas)
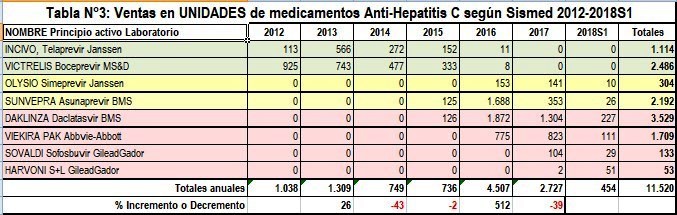
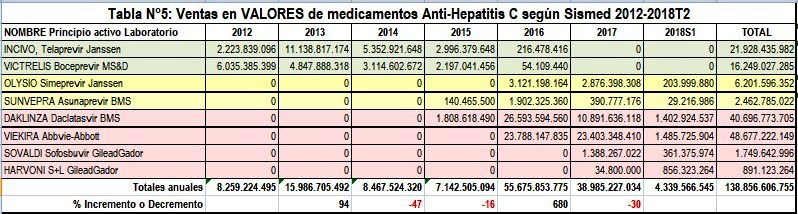
Según sus registros
sanitarios, Incivo® de Janssen, Victrelis® de Merck&Co-MS&D
y Olysio® de Janssen, ya fueron descontinuados, mientras
Sunvepra® de Bristol-Myers-Squibb y Viekira Pak® de
Abbvie-Abbott parecen tomar el mismo camino (según SISMED). Estos 5
antivirales anti-Hepatitis C se llevaron más de COP 130.000 millones
y se retiran por la innovación tecnológica, el advenimiento de
productos “pangenotípicos” (que tratan todos los genotipos del VHC y
no requieren genotipificación) y por la política pública de compras
centralizadas.
TELAPREVIR (Incivo® de Janssen)
ingresó el 2012 como una prometedora “innovación
terapéutica” y sus ventas subieron de COP 2.224
millones el 2012 a 11.139 millones el 2013. Luego,
bajaron a 5.353 millones el 2014, 2.996 millones el
2015 y solo 216 millones el 2016. Se retiró, pese a
estar vigente su “patente express” del Decreto 2085.
No incluido en el POS (hoy PBS), su precio -20
millones- se mantuvo sin regulación. Cuando su
registro sanitario mostró "Pérdida de Fuerza
Ejecutiva") Janssen había acumulado ventas por COP
21.928 millones.
BOCEPREVIR (Victrelis® de Merck&Co-MS&D),
vendió COP 6.035 millones el 2012, 4.848 millones el
2013, 3.115 millones el 2014, 2.197 millones el 2015
y solo 54 millones el 2016. Ese años caducó su
protección del Decreto 2085 y su registro sanitario
fue “Cancelado”. No incluido en el POS-PBS, su
precio -superior a 6,5 millones- no fue regulado.
Cuando se retiró, Merck&co-MS&D había acumulado
ventas por COP 16.249 millones.
SIMEPREVIR (Olysio® de Janssen),
cuya
autorización fue anulada por la EMA para la
Unión Europea, también tiene registro sanitario con
“pérdida de fuerza ejecutiva”. Su precio superó los
COP 20 millones y no fue regulado. Su protección del
Decreto 2085 tenía vigencia hasta agosto de 2020 y
cuando Janssen retiró este producto, había vendido
303 unidades por COP 6.181 millones.
ASUNAPREVIR (Sunvepra® de
Bristol-Myers-Squibb) no aparece entre los productos
registrados ante las agencias reguladoras de EEUU (FDA)
ni la Unión Europea (EMA)
pero fue evaluado favorablemente por el IETS y
obtuvo protección del Decreto 2085 (vigente hasta
agosto de 2020) pese a que el propio laboratorio
había retirado la NDA-New
Drug Applications 206844 ante la FDA, el 6 de
octubre de 2014. No incluido en el POS-PBS, su
precio tampoco fue regulado. Inició reportes de
precios y ventas a SISMED en 2015 y se retiraría
luego de vender 2.184 unidades por COP 2.454
millones.
La asociación ASUNAPREVIR+DACLATASVIR
(Sunvepra®)+Daklinza®, ambas de
Bristol Myers Squibb) estuvo autorizada para "uso
concomitante obligatorio" en infección por Virus
de la Hepatitis C genotipo 1B, lo cual ya fue
corregido en ambos registros sanitarios. Al
descontinuarse ASUNAPREVIR, DACLATASVIR permanecerá
en el mercado para uso asociado con SOFUSBUBIR, tal
como se incluyó en la compra centralizada promovida
por el Ministerio de Salud y la OPS.
La asociación fija DASABUVIR+OMBITASVIR+PARITAPREVIR+RITONAVIR
(Viekira Pak® de Abbvie-Abbott) aprobada por
la
FDA pero no por la
EMA (en la Unión Europea está registrada como
Ombitasvir+Paritaprevir+Ritonavir -Viekirax®
de Abbvie- sin Dasabuvir) reportó precios y ventas a
SISMED desde 2016 cuando vendió 23.788 millones. El
precio de la
caja de 56 tabletas alcanza para 4
semanas de tratamiento y supera
los 30 millones. El costo del tratamiento
promedio de 12 semanas supera los 92 millones (los
casos que requieran 24 semanas superan los
184 millones). Pese a lo
anterior, no
fue sometido a regulación de precios y en 2017 sus
ventas se mantuvieron en los 23.403 millones.
Tampoco fue incluido en el POS-PBS.
Aún sin estar registrada en la Unión
Europea, Viekira Pak® apareció en la “Guía
de práctica clínica para la tamización,
diagnóstico y tratamiento de personas con infección
por el virus de la hepatitis C” publicada por el
Ministerio de Salud en 2016, como un “esquema
preferido” con “recomendación fuerte, calidad
de la evidencia alta”.
Sin embargo, no apareció con la misma relevancia en
la “Vía
clínica para el tratamiento de hepatitis C crónica”
ni en los
Estudios previos de la compra centralizada,
que
hacen parte de las disposiciones de la
Resolución 1692
de 2017. Esta su exclusión del mecanismo de compra
centralizada, posiblemente sea responsable de la
disminución drástica de sus ventas reportadas, hasta
solo 1.486 millones en el primer semestre de
2018.
De seguir esta tendencia Viekira
Pak® -hasta hace poco el producto más vendido y
recobrado de este grupo- terminaría retirándose del
mercado luego de haberse llevado más de 48.000
millones.
-
Hepatitis C la primera
Política pública de compras centralizadas
Como dijimos en el primer párrafo, la
Resolución 1692
del 23 de mayo de 2017, constituye un sólido
documento de política pública, por las medidas que
adopta para la prescripción, compra centralizada,
distribución y suministro de medicamentos para la
Hepatitis C crónica. Su anexo técnico establece un
sistema de información para la
identificación de pacientes, diagnósticos y
tratamientos, que -con participación de la
Cuenta de Alto Costo CAC- está generando altos
niveles de
control en el seguimiento de esta
patología.
Los resultados del primer año de
implementación de la
Resolución 1692
aparecen resumidos en el
Boletín N°11 de 2018
ARMI
de la Cuenta de Alto Costo,
que en la página 4 dice: “La compra centralizada
no solo ha permitido la reducción de los costos del
sistema de salud (92 mil millones de pesos en la
primera compra), sino que también ha minimizado las
barreras en el acceso al tratamiento, ha limitado la
transmisión de la enfermedad, ha logrado la cura del
94,1% de los pacientes que hacen arte de la cohorte
de seguimiento y ha reducido la aparición de otras
hepatopatías” (gráfico N°3).
Gráfico N°3: Casos reportados a la
Cuenta de Alto Costo y Medicamentos prescritos
2017-2018
-
Futuro de las compras
centralizadas y la innovación tecnológica para
Hepatitis C
La
implementación de la
Resolución 1692
está resolviendo el problema de subregistro en la
notificación de casos con Hepatitis C Crónica en
SIVIGILA, está regulando la
prescripción,
distribución y suministro de los medicamentos y está
mejorando el sistema de información, identificación
de pacientes, diagnósticos y tratamientos. De
mantenerse esta política pública, estaríamos ante un
caso exitoso de racionalización de la prescripción y
control epidemiológico de una patología que
constituye una de las mayores amenazas para la
sostenibilidad financiera de nuestro sistema de
salud.
Además, el ingreso de asociaciones
como SOFOSBUVIR+LEDIPASVIR -ATC J05AP51- (Harvoni®
de Gilead-Gador), ELBASVIR+GRAZOPREVIR -ATC J05AP54-
(Zepatier® Merck Sharp & Dohme), SOFOSBUVIR+VELPATASVIR
-ATCJ05AP55- (Epclusa® de Gilead-Gador) y a
nivel internacional SOFOSBUVIR+VELPATASVIR+VOXILAPREVIR
-ATCJ05AP56- (Vosevi® de Gilead) y -aún sin
Código ATC- GLECAPREVIR+PIBRENTASVIR (Maviret®
de Abbvie) muestra una tendencia al parecer
irreversible -a nivel mundial- hacia los
tratamientos “pangenotípicos” que ofrecen la
posibilidad de tratar todos los genotipos del Virus
de la Hepatitis C, con mayor eficacia y seguridad,
sin necesidad de incurrir en los costos elevados de
los exámenes de genotipificación.
De mantenerse estas dos tendencias,
el escenario de una institucionalidad fortalecida
por el mecanismo de compras centralizadas,
negociando con el “pangenotípico” que ofrezca la
mejores condiciones científicas y económicas,
aparece como algo factible y podría resolver
temporalmente el problema de la Hepatitis C.
Pero, ésa no sería una solución
estructural porque las farmacéuticas ya acumularon y
siguen acumulando capacidades en “integración
profunda con dientes” con mecanismos de protección
de patentes y severidad regulatoria que ya están a
su servicio. Las farmacéuticas, cambiarán su actitud
negociadora tan pronto encuentren las condiciones
para hacerlo. Por lo tanto, la única solución
estructural está en fortalecer la aplicación de la
Resolución 1692 y avanzar en la declaratoria de
interés público con fines de licencia obligatoria.
Las soluciones propuestas por los
gremios farmacéuticos -en sus memoriales de
instrucciones para el nuevo gobierno- solo buscan
ampliar sus multimillonarias ganancias, a costa de
otro gran desastre para la salud pública en
Colombia.
|
|
4.
Compra centralizada de Medicamentos para Hepatitis C
Negociación y compra centralizada de
medicamentos. Espejo
página de MinSalud, el día 6 de agosto de 2018, antes
del cambio de gobierno
Ministerio de Salud y Protección Social > Salud > Medicamentos
y Tecnologías > Negociación y
compra centralizada de medicamentos
NOTA:
Añadimos enlaces a los archivos de reserva más importantes
https://youtu.be/irSaQ2MGVKY?list=PLdA3cVDe-LYz3UQ6K3qMwGJE_iJhVcUrs
La
Ley 1753 de 2015
https://bit.ly/2idwZ6C por la cual se
expide el Plan Nacional de Desarrollo
2014-2018 “Todos por un nuevo país”, en su
Artículo 71 se refiere a la negociación
centralizada de medicamentos, insumos y
dispositivos, modificando el Artículo 88 de
la Ley 1438 de 2011, quedando de la
siguiente manera
“ARTÍCULO 88. Negociación
centralizada de medicamentos,
insumos y dispositivos. El
Ministerio de Salud y Protección
Social (MSPS) establecerá los
mecanismos para adelantar
negociaciones centralizadas de
precios de medicamentos, insumos y
dispositivos. Los precios
resultantes de las negociaciones
centralizadas serán obligatorios
para los proveedores y compradores
de medicamentos, insumos y
dispositivos de servicios de salud y
estos no podrán transarlos por
encima de aquellos precios. El
Gobierno Nacional podrá acudir
subsidiariamente a la compra directa
de medicamentos, insumos y
dispositivos”.
El Ministerio de Salud y Protección
Social se encarga de la realización
de la negociación y compra
centralizada de medicamentos como
parte de las políticas orientadas a
garantizar el acceso a los
medicamentos por parte de la
población residente en el territorio
nacional, de la mano con las
acciones requeridas para contribuir
a la sostenibilidad financiera del
Sistema General de Seguridad Social
en Salud, en el marco de la garantía
del derecho fundamental a la salud.
Este espacio presenta los avances
normativos y demás información de
interés en dicho sentido.
Procesos de negociación y compra centralizada de medicamentos -
Hepatitis C crónica
Ruta
operativa
Ruta clínica
Eventos de socialización
•16nov17
BisBcm46de2017
Respuesta ADRES a Derecho
de Petición de FMC
Hepatitis C: Efectivamente VIEKIRA
PACK es el tratamiento más costoso y no es protagonista de compras
centralizadas
La Administradora de los Recursos del
Sistema General de Seguridad Social en Salud ADRES, en respuesta a
un derecho de petición de la Federación Médica Colombiana FMC,
confirmó que el xx% de los recobros efectivamente pagados por
medicamentos para Hepatitis C corresponde a la asociación fija
DASABUVIR + OMBITASVIR + PARITAPREVIR + RITONAVIR, comercializada
como VIEKIRA PAK de ABBVIE-ABBOTT
Videos
Hepatitis
C Diagnóstico y tratamiento
Oscar Beltrán, MD - Colombia XII Convención Nacional de la Asociación Colombiana de Hepatología Congreso Colombiano de Enfermedades Digestivas - ACADI 2015
| Publicado el 26 oct. 2015
Medicamentos contra la hepatitis C: el precio de estar sano | Global 3000
DW
Publicado el 9 jun. 2015 |
|
Envíenos sus aportes a
observamed.fmc@gmail.com |
|