|
1. Citación a la Comisión Intersectorial de Propiedad Intelectual.
La reunión de la CIPI fue convocada en realidad por AFIDRO
2. Acta de Reunión de la CIPI muestra actitud sesgada de la SIC:
2.1. Según la SIC la declaratoria de interés público que propone el Ministerio de Salud no tiene solidez técnica, es inconstitucional, resulta inútil en la práctica y expone al país a sanciones internacionales
2.2. "La licencia obligatoria debe versar sobre la patente como tal y no sobre un nombre comercial determinado"
2.3. Versión parcial y sesgada del Superintendente Delegado para la Propiedad Industrial
sobre la historia de esta patente
2.4. Visión sesgada del Superintendente Delegado para la Propiedad Industrial
sobre gama de productos con IMATINIB
2.5. Visión sesgada del Superintendente Delegado para la Propiedad Industrial
sobre inhibidores de tirosina quinasa
3. Conclusión: Funcionarios de la SIC que prejuzgaron sobre posibilidad de esta Licencia obligatoria deben marginarse del proceso.
El párrafo final que resume los
contenidos de los anteriores puntos, dice:
Por lo anterior, queda demostrado que por lo menos tres representantes de la Superintendencia
de Industria y Comercio, liderados por José Luis Londoño Fernández (Superintendente Delegado para la Propiedad Industrial)
participaron en la reunión de la Comisión Intersectorial de Propiedad Intelectual CIPI - Sesión Subcomisión de Propiedad
Industrial y presentaron solicitudes de aclaración o pedidos de solidez
técnica que se orientaron a imponer conceptos que finalmente fueron incorporados
como un anexo del Acta. Dicho Anexo contiene conceptos claramente sesgados en
contra de la posible declaratoria de interés público por parte del Ministro
de Salud e innegablemente favorables a los argumentos que esgrime Novartis en
defensa de la patente irregular de la forma cristalina beta de IMATINIB. Por
lo tanto -en la eventualidad de que el Ministro de Salud firme dicha
declaratoria de interés público y el expediente pase a la Superintendencia
de Industria y Comercio, para trámite de la licencia obligatoria- los
funcionarios que prejuzgaron y demostraron su falta de objetividad, deben
marginarse de dicho proceso, porque por su escaso interés en defensa del
interés público, no ofrecen ninguna garantía de justicia y probidad.
2.
Los "hechos" del Anexo A de la respuesta de Novartis al Ministerio
de Salud
La respuesta
de Novartis al Ministerio de Salud,
trae además un Anexo A donde se plantean los siguientes "hechos":
2.1.
"Novartis nunca ha tenido el monopolio de Imatinib en Colombia. Existen actualmente otras 2 compañías farmacéuticas que comercializan productos de
Imatinib en Colombia, que no infringen la patente de Novartis"
Este planteamiento de Novartis puede ser parcialmente cierto, pero, es
contradictorio con lo planteado por el tantas veces mencionado Superintendente Delegado para la Propiedad
Industrial que -para defender la misma tesis de que existe competencia en este
mercado- habla de "un total de veintiséis (26) registros sanitarios"
con el principio activo IMATINIB..."siete (7) de ellos se encuentran actualmente vencidos, pero sin embargo dos (2) de ellos se encuentran en trámite de renovación y los
diecisiete (17) restantes se encuentran vigentes" dice (ver
Anexo Acta pag.10-11).
¿Por qué estos datos son tan
discrepantes? Podría ser, porque Londoño Fernández hizo estudios de
escritorio y quienes elaboraron el documento de Novartis saben lo que pasa en
el campo. Alguien teoriza y alguien sabe lo que pasa en la realidad y ambos
pueden tener parte de la razón: Sí, alcanzaron a registrarse hasta 26
productos con IMATINIB, pero casi todos los competidores fueron eliminados y
podría tener razón Novartis si considera que solo quedan dos compañías
farmacéuticas que significan algún grado de competencia.
Lo anterior
nos lleva a matizar la primera parte de la afirmación: Es posible que no
exista monopolio en el sentido estricto de la palabra, pero ¿no existirán
prácticas de abuso de posición dominante o relaciones fácticas de mercados
monopólicos?. Los funcionarios de la Superintendencia de Industria y Comercio
deberían salir al campo a investigar esa posibilidad. Active
este hipervínculo para ver más detalles sobre este punto.
2.2.
"La existencia de la patente de Glivec® no afecta el acceso de los pacientes al tratamiento. La molécula hace parte de los tratamientos para Leucemia Mieloide Crónica incluidos en el Plan Obligatorio de
Salud"
Otro planteamiento de Novartis que puede ser parcialmente cierto, porque
IMATINIB efectivamente está incluido en el POS. Pero, afirmar que los altos
costos derivados de la patente de Glivec no afectan el acceso de los pacientes
a sus medicamentos, constituye una falacia que ofende la razón. Peor aún,
afirmar que la inclusión de este medicamento en el POS garantiza el acceso de
los pacientes al mismo, implica un grave desconocimiento del estado en que se
encuentra el sistema de salud colombiano.
Lo cierto es que los sobrecostos
ligados a la patente de Glivec, estimados por el Ministerio de Salud como
ahorro generado por la posible licencia obligatoria, bordean los 100.000
millones. Afirmar que semejante suma -convertida en ganancia para Novartis por
la patente- no afecta el acceso de los pacientes a sus tratamientos porque
Imatinib está incluido en el Plan Obligatorio de Salud, es simplementre
absurdo.
El viejo cuento de que el precio
de los medicamentos no importa, porque el sistema los paga -vía UPC si está
en el POS, o vía recobro si no está- es ya infantil.
Insistir con este argumento -como también lo hace el actual director de
AFIDRO que hasta hace poco dirigió la Superintendencia de Salud- es
simplemente vergonzoso.
2.3. Los demás
"hechos" plateados en la respuesta de Novartis son:
- "El precio de venta de Glivec® no es el resultado de una decisión del fabricante. Desde el 2011, el precio de
Glivec® ha sido fijado y controlado por el Gobierno"
- "Declarar el Interés Público sobre la patente de Glivec® no es una solución a los desafíos financieros estructurales del sector salud"
y
- "No existen amenazas de abastecímiento de Imatinib. Novartis siempre ha garantizado el
abastecimiento adecuado e ininterrumpido del tratamiento"
Precisamente, el "Informe
sobre la recomendación al ministro de salud y protección
social en relación con la solicitud de declaratoria de
interés público del IMATINIB con fines de licencia
obligatoria" reconoce
que la regulación de precios no fue suficiente (AR).
Es verdad que la declaratoria de interés público sobre la patente de Glivec
no resolverá los desafíos financieros estructurales del sector salud, pero
-sin duda- constituye un paso en la dirección correcta. Y lo último ¿a qué
se refiere con la amenaza de desabastecimiento?.
3.
Propuesta de COP 140/mg rechazada por Novartis es muy superior al precio/mg promedio reportado por
competidores.
SISMED de 2015 muestra "competencia real" de COP 68/mg como precio/mg
promedio de competidores de GLIVEC 400 mg
|
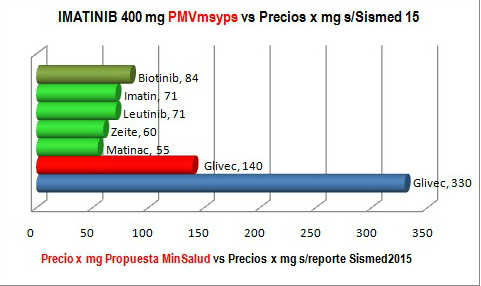
Gráfico N°1: Precio por mg de IMATINIB según
reportes a Sismed 2015
 |
Como ya se
dijo, el "Informe
sobre la recomendación al ministro de salud y protección
social en relación con la solicitud de declaratoria de
interés público del IMATINIB con fines de licencia
obligatoria" (ARMI)
dice que debe negociarse con la multinacional Novartis,
bajo la premisa de que el precio de "Glivec® debe bajar hasta el punto de una competencia
simulada".
En el Análisis
técnico de la oferta de MinSalud (AR)
puede verse la técnica empleada para el cálculo del
"punto de competencia simulada", pero, al margen de dicha
técnica -empíricamente-
puede decirse que existe además un "punto de competencia real" como
el resultado del precio promedio del miligramo de IMATINIB reportado a
SISMED del año 2015 por los competidores de GLIVEC 400 mg. El
gráfico N°1 muestra que -de acuerdo con dichos reportes- el precio/mg promedio reportado por competidores de GLIVEC 400 mg el año 2015
fue de COP 68/mg (promedio de los precios/mg de Biotinib, Imatin,
Leutinib, Zeite y Matinac de 400 mg). Por
lo tanto, puede decirse que la propuesta del Ministerio de Salud,
resultaba más que razonable para Novartis, pero como ya se dijo en el
Boletín
N°16 existen razones estratégicas de esta multinacional, que al
margen de cualquier consideración de "responsabilidad
social" hacen primar su interés comercial. |
En conclusión, el rechazo de la
propuesta del Ministerio de Salud por parte de Novartis estaba previsto, como
previsto está que utilizará todos los medios a su alcance para -en la
eventualidad de que el Ministro Gaviria firme la declataroria de interés
público- interferir en el trámite de la licencia obligatoria, que
adicionalmente ya tiene en contra las "interpretaciones" sesgadas a
favor de Novartis de los
funcionarios que ya prejuzgaron y demostraron su falta de objetividad.
Funcionarios que como ya dijimos, deben
marginarse de este proceso, porque no ofrecen ninguna garantía de justicia y probidad.
| Caso
IMATINIB: Conozca más de la vigilancia activa de OBSERVAMED-FMC y el
CNQFC |
|
Iniciativa Vigilancia
Activa de Observamed-FMC-CNQFC
N°27
Comité
especial declaró IMATINIB
de interés público y recomendó
a Ministro de Salud
Licencia Obligatoria si GLIVEC®
Novartis no ofrece precios de competencia
http://www.med-informatica.net/BIS/BisBcm10de2016_29feb06mar16.htm
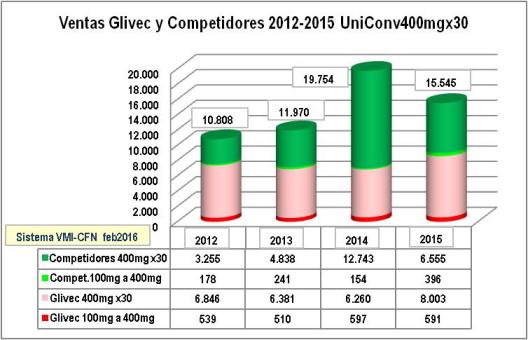
El consumo anual de IMATINIB 2012a15 se incrementó en 50%
Gráfico
N°1: Evolución ventas Glivec
y competidores s/Sismed 2012-2015
Iniciativa Vigilancia
Activa de Observamed-FMC-CNQFC
N°32
Primera
propuesta de MinSalud a Novartis:
Nuestra debilidad
institucional frente a la estrategia mundial y falsa
responsabilidad social de esta multinacional
http://www.med-informatica.net/BIS/BisBcm16de2016_11a17abr16.htm
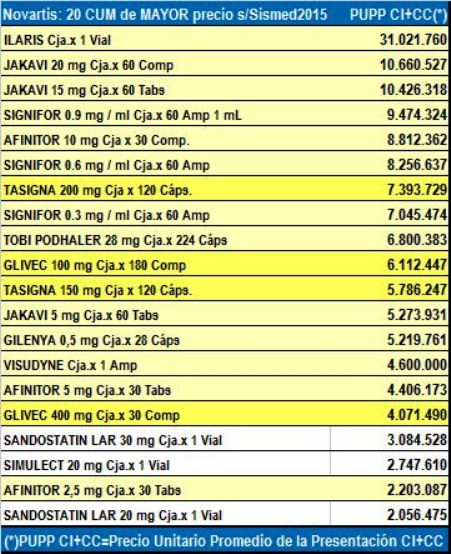
Novartis y su gran viraje hacia medicamentos de alto costo
Gráf.N°1:
Precio Unitario Promedio de Presentación de 20 CUM Novartis
 |
Iniciativa
Vigilancia
Activa de Observamed-FMC-CNQFC
N°31
Interés público de IMATINIB: Superintendente Delegado
para la Propiedad Industrial emite concepto impreciso y sesgado a favor de Novartis
y contrario a MinSalud
http://www.med-informatica.net/BIS/BisBcm14de2016_28mar03abr16.htm
Reunión de la CIPI fue
convocada en realidad por AFIDRO
Gráfico
N°1: AFIDRO y la convocatoria a reunión extraordinaria CIPI

____________________________________________________
Comité de Veeduría y Cooperación en Salud
COMUNICADO-20abr16
-
COMUNICADO-26abr16

|
ALGUNAS NOTAS RECIENTES DE PRENSA:
http://www.elespectador.com/opinion/juego-de-tronos-tercera-temporada
http://www.elespectador.com/opinion/editorial/salud-mas-alla-del-negocio-articulo-629398
http://www.elespectador.com/noticias/salud/otra-traba-tendran-los-pacientes-leucemia-medicamentos-articulo-629518
http://www.elespectador.com/noticias/salud/novartis-perderia-exclusividad-fabricar-imatinib-medica-articulo-629267
http://www.opinionysalud.com/organizaciones-civiles-piden-al-minsalud-no-dilatar-mas-la-licencia-publica-imatinib/
http://www.noticiasrcn.com/nacional-pais/enfrentamiento-entre-minsalud-y-laboratorio-internacional-patente-medicamento-contra
http://www.lafm.com.co/salud/noticias/alejandro-gaviria-ministro-de-204799
http://caracol.com.co/radio/2016/04/26/salud/1461694317_750936.html
http://www.elcolombiano.com/colombia/salud/gobierno-pide-retirar-patente-de-medicamento-contra-el-cancer-a-novartis-JF4043182
http://www.vanguardia.com/colombia/356134-minsalud-pedira-retirar-patente-de-medicamento-contra-la-leucemia-a-novartis
http://www.elpais.com.co/elpais/colombia/noticias/minsalud-pedira-retirar-patente-medicamento-para-tratar-leucemia-novartis
Envíe sus aportes y
comentarios a observamed.fmc@gmail.com
o trine con @OBSERVAMED
Sobre
conflictos de interés:
La iniciativa "Elijamos
Sabiamente" de la Federación
Médica Colombiana FMC y el Colegio
Nacional de Químicos Farmacéuticos de Colombia CNQFC, no recibe ninguna retribución monetaria, ni en
especie, de ninguna entidad pública ni privada, que pueda comprometer
la independencia de sus investigaciones e informes.
Participe
escribiéndonos a observamed.fmc@gmail.com
|