| El
año 2012 se reportó únicamente la venta de 1 unidad de 1,2 mg
(CUM 19906409-01 cuyo registro sanitario estaba vencido desde el
7 de julio de 2010) y esa inconsistencia podía atribuirse a
problemas en el paso de la comercialización de este producto de
Amarey NovaMedical al propietario real del producto, la
multinacional NovoNordisk. La hipótesis de que el reporte de
17,3 gramos de 2013 incluiría las ventas no reportadas del 2012
y no correspondería a un verdadero incremento de las ventas en
unidades, quedó pulverizada con el incremento del año 2014: El
paso a 35,7 gramos que casi quintuplica el
promedio de los años 2008 a 2011, no es explicable ni por
ajustes en reportes, ni aumento de pacientes (básicamente son
los mismos) y ni siquiera por incremento del uso profiláctico.
En efecto, si asumimos que las
indicaciones aprobadas para este producto siguen siendo "TRATAMIENTO DE EPISODIOS DE HEMORRAGIA Y PARA LA PREVENCIÓN DE LA HEMORRAGIA EN PACIENTES SOMETIDOS A CIRUGÍA O A PROCEDIMIENTOS INVASIVOS DENTRO DE LOS SIGUIENTES GRUPOS: VIII O IX >5BU. EN PACIENTES CON HEMOFILIA CONGÉNITA EN LOS QUE SE PREVÉE UNA ALTA RESPUESTA ANAMNÉSICA A LA ADMINISTRACIÓN DE FACTOR VIII O FACTOR IX. EN PACIENTES CON HEMOFILIA ADQUIRIDA. EN PACIENTES CON DEFICIENCIA CONGÉNITA EN FACTOR VII. EN PACIENTES CON TROMBASTENIA DE GLANZMANN CON ANTICUERPOS Y REFRACTARIOS ANTERIOR O ACTUALMENTE A LAS TRANSFUSIONES DE PLAQUETAS. PROFILAXIS EN PACIENTES CON HEMOFILIA CON
INHIBIDORES" no existe ninguna razón epidemiológica
que justifique el incremento del consumo promedio anual de 7,5
gramos, a 17,3 gramos el 2013 y hasta 35,7 gramos el 2014.
Obviamente, la farmacéutica, las EPS que manejan los recobros
con este medicamento y las autoridades encargadas de vigilancia
y control, le deben una buena explicación al país.
2.
Los años 2008 a 2011 NOVOSEVEN vendió en promedio COP 36.949
millones. El año 2013 registró un incremento de +84% y
el año 2014 +31% sobre dicho promedio
|
|
Gráfico
N°2: Evolución ventas reportadas NOVOSEVEN en COP (millones)
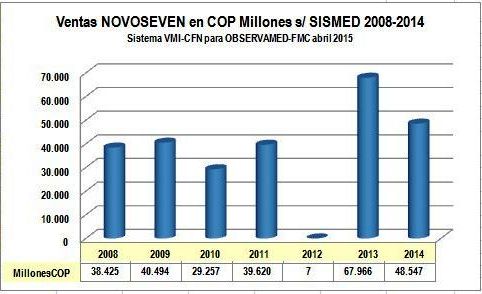 |
El Gráfico
N°2 muestra cómo las ventas de este medicamento en el período
2008-2011 (sin regulación de precios) se mantuvieron en un
promedio de COP 36.949 millones.
El año 2012 no se reportaron
ventas posiblemente por problemas en el paso de la
comercialización de este producto de Amarey NovaMedical al
propietario real del producto, la multinacional NovoNordisk.
Alguien tendrá que explicar lo sucedido.
Las ventas reportadas por
NovoNordisk a SISMED del año 2013 alcanzaron la suma de COP 67.966
millones. Es decir, tuvieron un incremento de +84%
sobre el promedio de los años 2008 a 2011, lo cual -como sucede
con las ventas en mg- tampoco se justifica por variables
epidemiológicas.
En el gráfico N°2, también
puede verse que el volumen de ventas del año 2014 registra un
incremento de +31% sobre el promedio de los años 2008 a
2011, pese a grandes variaciones de precios y ventas en mg que
pueden verse en los gráficos N°1 y N°3. |
3.
La farmacéutica
obtuvo mejores resultados pese a que la nueva
regulación redujo dramáticamente los precios
|
Gráfico N°3: Evolución costos por mg de NOVOSEVEN en COP (millones)
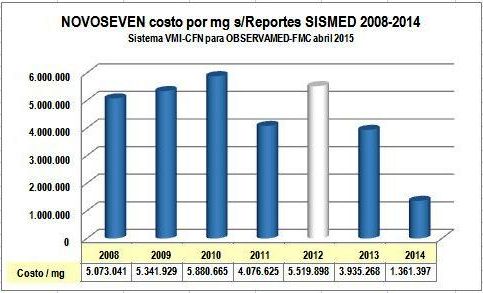 |
El Gráfico
N°3 muestra que el precio por mg, además de muy alto (superior
a COP 5 millones) fue creciente los años 2008 a 2010. En
el detalle de los reportes,
de esos años, Amarey Novamedical reportó ventas solo por canal
comercial y el año 2011 reportó por ambos canales. El precio
por mg bajó a COP 4 millones (el año 2012 no se incluye en el
análisis porque corresponde a 1 unidad).
En el mismo detalle de reportes
puede verse que el año 2013 comienza la comercialización por
NovoNordisk que reporta solo las presentaciones de 1 y 2 mg y
solo por canal institucional. El precio por mg se mantiene
prácticamente igual a los 4 millones del año 2011 y el gran
incremento de unidades (gráfico N°1) se refleja en el
resultado extraordinario de ese año (gráfico N°2).
El año 2014 se hace efectiva la
nueva regulación de precios y el precio por mg se reduce a COP
1,4 millones (gráfico N°3) pero el extraordinario incremento
de ventas en mg (gráfico N°1) se refleja en un resultado que
de todas maneras es superior (+31%) al promedio de los
años 2008 a 2011 (gráfico N°2). |
4.
La solución está en ampliar la regulación de precios con
políticas públicas de transparencia y participación social
El caso de los Factores Antihemofílicos y la Hemofilia en general fue
presentado por la FMC como emblemático
de la debilidad institucional para controlar los excesos de las
farmacéuticas y las EPS-IPS intermediarias en los recobros al FOSYGA.
La misma FMC, además de denunciar
los precios exorbitantes de estos productos y las irregularidades en sus
recobros (ver BisBcm43de2010),
criticó la insuficiencia de la primera regulación basada en Valores
Máximos de Recobro VMR (ver BisBcm09de2011).
Pese a que la FMC demostró que los VMR
eran muy superiores al promedio de 20 países de la Federación Mundial
de Hemofilia los VMR de la Resolución 05 de 2011 fueron ratificados
pos las Resoluciones 1020 y 3026 de 2011, así como por 3470 de 18ago2011,
4316 de 27sep11, 2569 de 30ago12 y finalmente la Circular 04 de 2012.
Felizmente para el bien del país, la
nueva regulación de precios basada en precios de referencia
internacional (Circular 03 de 2013) rectificó
esta situación y el precio regulado de cada mg pasó de COP 6.182.287
a COP 1.592.311 (incluido el porcentaje de prestadores). La FMC reconoció
este cambio y lo calificó como "un
paso en la dirección correcta".
Ya en el campo del manejo de la Hemofilia
en Colombia, además de la nueva regulación de precios, el Ministerio
de Salud y Protección Social publicó el PROTOCOLO CLÍNICO PARA TRATAMIENTO CON PROFILAXIS DE PERSONAS CON HEMOFILIA A SEVERA SIN INHIBIDORES
(AR)
y expidió la Resolución 123 de 2015
(AR)
que estableció el reporte de información de pacientes diagnosticados con hemofilia y otras coagulopatías asociadas a déficit de factores de la coagulación a la
Cuenta de Alto Costo por parte de las Instituciones Prestadoras de Salud (IPS) y
Empresas Administradoras de Planes de Beneficio (EAPB), incluyendo regímenes de excepción y especiales.
Este reporte deberá realizarse a más tardar el 30 de marzo de cada año, con la medición de 90 variables relacionadas con aspectos correspondientes a la identificación, diagnóstico, otras ayudas diagnósticas iniciales, antecedentes para hemofílicos, tratamiento inicial y actual, hemorragias, complicaciones, manejo multidisciplinario, urgencias y
hospitalizaciones. Lo anterior servirá como insumo base para la consolidación de esta información y permitirá realizar análisis de identificación, ubicación, concentración y manejo de los pacientes a través de la estandarización de mediciones, monitoreo y evaluación por resultados en
salud" dice el ministerio en una nota de prensa sobre el reconocimiento
de la Federación Mundial de Hemofilia a esta labor.
Adicionalmente, la Mesa de Hemofilia (donde
actúan el ministerio, cuenta de alto costo, sociedades científicas de
hematología adultos, pediátrica, ortopedia, ortopedia infantil,
además de fisiatría, enfermeros, odontólogos y la liga de
hemofílicos como asociación de pacientes) funciona como un ente asesor
del Ministerio de Salud en la definición de políticas públicas en
este campo. Por lo tanto, existe una posibilidad cierta de adelantar
acciones que vayan más allá de la simple regulación de
precios y superen nuestra evidente debilidad institucional para identificar y
controlar posibles prácticas de inducción a la demanda y litigio
inducido.
Si estas políticas públicas se
trasladan a otras patologías y al sistema de salud en su conjunto,
podemos decir que existen soluciones factibles y que su implementación
exitosa, es lo único que puede detener y revertir, la actual marcha
inexorable hacia la inviabilidad del sistema.
|